$A$. જયારે $H$ એ સહસંયોજક રીતે ખુબ જ ઊચા વિધુતઋણમય પરમાણુ સાથે બંધ બનાવે છે ત્યારે હાઈડ્રોજન બંધ અસ્તિત્વ ધરાવે છે.
$B$. $૦-$નાઇટ્રો ફીનોલ માં આંતરઆણ્વીય $H$ બંધ હાજર છે.
$C$. $HF$ માં આંત:આણ્વીય $H$ બંધ હાજર છે.
$D$. સંયોજન ની ભોતિક અવસ્થા પર $H$ બંધ ની માત્રા આધારિત છે.
$E$. સંયોજનો ના બંધારણ અને ગુણધર્મો પર $H-$ બંધ શક્તિશાળી અસર ધરાવે છે.
નીચે આપેલા વિકલ્પો માંથી સાચો જવાબ પસંદ કરો.
$(A)$ Generally hydrogen bonding exists when $\mathrm{H}$ is covalently bonded to the highly electronegative atom like $\mathrm{F}, \mathrm{O}, \mathrm{N}$.
$(B)$ Intramolecular $\mathrm{H}$ bonding is present in
(Image)
$(C)$ Intermolecular Hydrogen bonding is present in $\mathrm{HF}$
$(D)$ The magnitude has Hydrogen bonding in solid state is greater than liquid state.
$(E)$ Hydrogen bonding has powerfull effect on the structure & properties of compound like melting point, boiling point, density etc.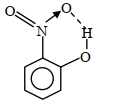
Download our appand get started for free
Similar Questions
- 1View Solutionરાસાયણિક બંધનને ધ્યાનમાં રાખીને નીચેના પરમાણુ માટે યોગ્ય વિકલ્પ પસંદ કરો
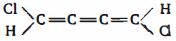
- 2સૂચિ $I$ સાથે સૂચિ $II$ ને જોડો.View Solution
સૂચિ $-I$ સૂચિ $-II$ $(A)$ $\Psi_{ MO }=\Psi_{ A }-\Psi_{ B }$ $(I)$ દ્વિધ્રુવ ચાકમાત્રા $(B)$ $\mu=Q \times I$ $(II)$ બંધકારક આણ્વિય કક્ષક $(C)$ $\frac{N_{b}-N_{a}}{2}$ $(III)$ બંધપ્રતિકારક આણ્વિય કક્ષક $(D)$ $\Psi_{ MO }=\Psi_{ A }+\Psi_{ B }$ $(IV)$ બંધક્રમાંક નીચે આપેલા વિકલ્પોમાંથી સાચો જવાબ પસંદ કરો.
- 3View Solutionબંધ ક્રમાંક ...... માં મહત્તમ છે.
- 4View Solutionઆલ્કલી ધાતુ આયનોની જલીયકરણ એન્થાલ્પીનો સાચો ક્રમ જણાવો.
- 5ઘન $XeF_6$ના ધનાયન ભાગમાં $Xe$ના સંકરણની સ્થિતિ શું છે?View Solution
- 6View Solutionદ્વિધ્રુવ ચાકમાત્રાને આધારે નીચેના અણુઓની ગોઠવણીમાંથી કઇ ગોઠવણી સાચી છે?
- 7View Solutionનીચે આપેલ કયા અણુના કેન્દ્રિય અણુના સંકરણની સ્થિતિ અન્ય અણુની જેવી નથી
- 8નીચેના વિધાનો માટે આરંભિકનો યોગ્ય ક્રમ $ T $ અથવા $F$ આપો. જો વિધાન સાચું હોય તો $T$ અને જો ખોટું હોય તો $F$ નો ઉપયોગ કરો:View Solution
$(I)$ ઇલેક્ટ્રોનની જુદી જુદી જોડી વચ્ચે અપાકર્ષણનો ક્રમ $l_P - l_P > l_P - b_P > b_P - b_P$ છે$(II)$ સામાન્ય રીતે, જેમ જેમ કેન્દ્રીય અણુ પર અબંધકારક ઇલેક્ટ્રોન યુગ્મની જોડીની સંખ્યા વધે છે,સામાન્ય બંધખૂણાથી બંધખૂણા નું મૂલ્ય પણ વધે છે.
$(III)$ $H_2O$માં $O$ પર અબંધકારક ઇલેક્ટ્રોન યુગ્મ $2$ છે જ્યારે $NH_3$માં $N$ પર $1$ છે
$(IV)$ ઝેનોન ફ્લોરાઇડ્સ અને ઝેનોન ઓક્સીફ્લોરાઇડ્સના બંધારણોને $VSEPR$ સિદ્ધાંતના આધારે સમજાવી શકાયું નહીં
- 9View Solutionનીચે આપેલા અણુ/આયનોની કઇ જોડમાં બંને ઘટકો અસ્તિત્વમાં હોવાની શક્યતા નથી?
- 10નીચેના કયા અણુમાં સૌથી ઓછી $O-O$ બંધ લંબાઈ છે?View Solution
