$A _2+ B _2 \rightarrow 2 AB ; \Delta H _{ r }^0=-200\,kJ\,mol ^{-1}$
$\Rightarrow \Delta H _{ p }^0( AB )=-200\,kJ\,mol\,m ^{-1}$
$\therefore \Delta H _{ R }^0$ for reaction $A _2+ B _2 \rightarrow 2 AB$ is $-400\,kJ\,mol ^{-1}$
Given: Bond Enthalpy of $A _2, B _2$ and $AB$ is $1: 0.5: 1$
Assuming bond enthalpy of $A _2$ be $x\, kJ\, mol { }^{-1}$
$\therefore$ Bond enthalpy $B _2=0.5 \times kJ\, mol ^{-1}$
$\therefore$ Bond enthalpy $AB =( x ) kJ\, mol\, m ^{-1}$
$-400= x +0.5 x -2 x$
$-400=-0.5 x$
$\therefore x =800\,kJ / mol$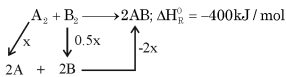
Download our appand get started for free
Similar Questions
- 1ઇથિલિનના ચોક્કસ જથ્થાનું દહન કરતા $6226\, kJ$ ઉષ્મા ઉત્પન્ન થાય છે. જો તેની દહન-એન્થાલ્પી $1411\, kJ\, mol^{-1}$ હોય, તો $STP$ એ પ્રક્રિયામાં વપરાયેલા ઓક્સિજન પરમાણુઓની સંખ્યા ...............${N_A}$ થશે.View Solution
- 2$XY, X_2$ અને $Y_2$ (બધા દ્રીપરમાણ્વિય અણુઓ) ની બંધવિયોજન ઊર્જા $1:1 : 0.5$ ગુણોતરમાં છે. અને $XY$ ની સર્જનઉષ્મા $(\Delta _fH)$ $-200 \,kJ\, mol^{-1}$ છે. તો $X_2$ ની બંધવિયોજન ઊર્જા કેટલા ......$kJ\,mo{l^{ - 1}}$ થશે ?View Solution
- 3બળતણ કોષમાં મિથેનોલ બનતણ તરીકે અને ઓક્સિજન ઓક્સિડેશનકર્તા તરીકે વર્તે છે. પ્રક્રિયા નીચે મુજબ છે.View Solution
$CH_3OH(l)+ \frac{3}{2} O_2 (g)$$ \rightarrow CO_2 (g)+ 2H_2O(l)$
$298\, K$ પર $CH_3OH(l),H_2O(l)$ અને $CO_2 (g)$ ની પ્રમાણિત સર્જન મુક્તઊર્જા અનુક્રમે $-166.2,-237.2$ અને $-394.4\, kJ\,mol^{-1}$ છે. જો મિથેનોલની પ્રમાણિત દહન એન્થાલ્પી $-726 \,kJ\, mol^{-1}$ હોય, બળતણ કોષની કાર્યક્ષમતા ......... $\%$ જણાવો.
- 4$298\,K$ એ $N_{2(g)} + 3H_{2(g)} \rightarrow 2NH_{3(g)}$ પ્રક્રિયા માટે એન્થાલ્પી ફેરફાર ($\Delta H$) $-92.38\, kJ$ છે. તો $298\,K$ એ આંતરિક ઉર્જાનો ફેરફાર ($\Delta U$) કેટલા ...... $kJ$ હશે ?View Solution
- 5એક આદર્શ વાયુ ના ત્રણ moles ને $5$ atm ના અચળ દબાણ નો ઉપયોગ કરીને સમ તાપીય રીતે $60 \mathrm{~L}$ થી $20 \mathrm{~L}$ દબાવવામાં (સંકોચવામાં) આવ્યો. આ સંકોચન માટે ઉષ્મા વિનિયમ $Q$ એ - ............. Lit. atm છે.View Solution
- 6$C + O_2$ $\rightarrow$ $CO_2$ : $\Delta H$ = $-x$ કિલોજૂલ, $2CO + O_2$ $\rightarrow$ $2CO_2$ : $\Delta H^° = -y$ કિલોજૂલ હોય, તો કાર્બન મોનેક્સાઈડની સર્જન એન્થાલ્પી (સર્જન ઉષ્મા) શોધો.View Solution
- 7$3O_2$ $\rightarrow$ $2O_3$ ; $\Delta H =$ ઘન પ્રક્રિયાને ધ્યાનમાં લેતાં, તો પ્રક્રિયા પરથી આપણે શું કહી શકીએ ?View Solution
- 8$(298\, K)$ એ મિથેનોલનું $\Delta H{^o _f}$ એ નિચેની કઈ રાસાયણિક સમીકરણ દ્વારા આપવામાં આવે છેView Solution
- 9View Solutionસાચો ઉત્તર પસંદ કરો. ઉષ્માગતિય અવસ્થા વિધેય .............. રાશિ છે.
- 10View Solutionનીચેના પૈકી ક્યુ સમીકરણ, આદર્શ વાયુને સમાવતા આપેલા પ્રક્રમ માટે ઉષ્માગતિશાસ્ત્રના પ્રથમ નિયમને રજૂ કરતું નથી ?
