$(A)\, n = 5, m_l= + 1$ $(B)\, n =2, l =1, m_l= -1, m_s = -1/2$ આપેલ છે . તો $(A)$ અને $(B)$ માં આપેલ ક્વોન્ટમ આંક મુજબ પરમાણુમા ઇલેક્ટ્રોનની મહતમ સંખ્યા અનુક્રમે જણાવો
JEE MAIN 2013, Medium
b
\((i)\) \(n=5\) means \(l=0,1,2,3,4\)
\((i)\) \(n=5\) means \(l=0,1,2,3,4\)
since \(m= +1\)
hence total no. of electrons will be \(= 0\) (from \(s\)) \(+ 2\) (from \(p\)) \(+ 2\) (fron \(d\)) \(+ 2\) (from \(f\)) \(+ 2\) (from \(g\))
\(=0+2+2+2+2=8\)
\((ii)\) \(n=2,\,l=1,\,m_l=-1,\,m_s=-1/2\) represent \(2p\) orbital with one electron
Download our appand get started for free
Experience the future of education. Simply download our apps or reach out to us for more information. Let's shape the future of learning together!No signup needed.*
Similar Questions
- 1$Li ^{2+}$ ની $3^{\text {rd }}$ અને $4^{\text {th }}$ કક્ષક વચ્ચેનો તફાવત $\Delta R _{1}$ છે. $He ^{+}$ ની $3^{\text {rd }}$ અને $4^{\text {th }}$ કક્ષક વચ્ચેનો તફાવત $\Delta R _{2}$ છે.$\Delta R _{1}: \Delta R _{2}$નો ગુણોતર :View Solution
- 2સુચિ $I$ સાથે સુચિ $II$ ને જોડો.View Solution
List $I$ (હાઈડ્રોનન માટે વાર્ણપટશ્રેણીઓ ) List $II$ (વાર્ણપટ વિસ્તાર / ઉચ્ચ(ઉંચી) ઉર્જા અવસ્થા) $A$. લાયમન $I$. પારરકત વિસ્તાર $B$. બમાર $II$. $UV$ વિસ્તાર $C$. પાશ્વન $III$. પારરકત વિસ્તાર $D$. ફૂંડ $IV$. દ્રશયમાન વિસ્તાર નીચે આપેલ વિકલ્પોમાંથી સાચો જવાબ પસંદ કરો.
- 3View Solutionતરંગવિધેયનો રેડિયલ ભાગ ક્યા ક્વોન્ટમ આંક વડે દર્શાવાય છે ?
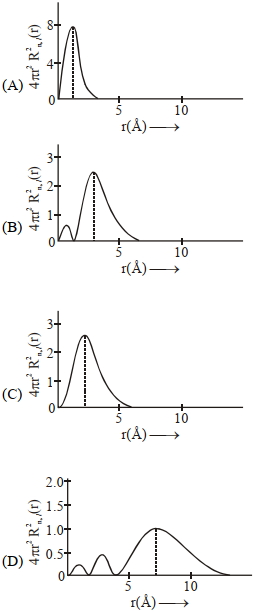
- 4હાઈડ્રોજન પરમાણુની વિવિધ કક્ષકો માટે ત્રિજ્યા વિતરણ વિધેય વિરુદ્ધ $'r'$ ના આલેખ નીચે આપેલ છેView Solution
${image}$
તો, $3s$ કક્ષક માટે સાચો આલેખ શોધો
- 5View Solutionહાઈડ્રોજન સ્પેક્ટ્રમની રેખાની બોહર શ્રેણીમાં, લાલ છેડેથી ત્રીજી રેખાને અનુલક્ષે છે જે નીચેના કયા આંતર-ભ્રમણકક્ષામાંથી એક બોહર માટે અણુમાં ભ્રમણ કરે છે...
- 6નીચેનામાંથી કયા સિદ્ધાંતો$/$નિયમો ભ્રમણકક્ષામાં ઇલેક્ટ્રોનની મહત્તમ સંખ્યાને બે સુધી મર્યાદિત કરે છે?View Solution
- 7View Solutionમુખ્ય ,એજીમ્યુથલ અને ચુંબકીય ક્વોંટમ નંબર કોને અનુક્રમે છે ?
- 8View Solutionહાઇડ્રોજન પરમાણુના સંદર્ભમાં કયું વિધાન સાચું ?
- 9નીચે બે વિધાનો આપેલા છે, એકને કથન $A$ તરીક અને બીજાને કારણ $R$ તરીકે લેબલ કરેલ છે.View Solution
કથન $A$ : હાઈડ્રોજન પરમાણુની $2s$ કક્ષકની ઊર્જા લિથિયમની $2s$ કક્ષકની ઊર્જા કરતા વધુ છે.
કારણ $R$ : એક જ પેટાકોશમાં આવેલી કક્ષકોની ઊર્જાઓ પરમાણુ ક્રમાંક વધવાની સાથે
ઉપરોક્ત વિધાનોના સંદર્ભે નીચેના વિકલ્પોમાંથી યોગ્ય ઉત્તર પસંદ કરો.
- 10રીડબર્ગ અચળાંક $\left(\mathrm{R}_{\mathrm{H}}\right)$ નું મૂલ્ય $2.18 \times 10^{-18} \mathrm{~J}$ છે. હાઈડ્રોજન પરમાણુની બહોરની પ્રથમ કક્ષામાં $9.1 \times 10^{-31} \mathrm{~kg}$ દળ ધરાવતા ઈલેટ્રોન નો વેગ = ........... $\times 10^5 \mathrm{~ms}^{-1}$ છે. (નજીકનો પૂણાંક)View Solution
