$2N_2O_5 (g) \to 4NO_2 (g) + O_2 (g)$
$N_2O_5$ ની શરૂઆતની સાંદ્રતા $3.00\, mol\, L^{-1}$ છે. અને $30$ મિનિટ બાદ તે $2.75\, mol\, L^{-1}$ છે. તો $NO_2$ તા સર્જનનો દર ................ $mol\, L^{-1}\, min^{-1}$ જણાવો.
\(2N_2O_5 (g) \to 4NO_2 (g) + O_2 (g)\)
\(t=0\) \(3.0\,M\)
\(t=30\) \(2.75\,M\)
\(\frac{{ - \,\Delta \,[{N_2}{O_5}]}}{{\Delta t}}\, = \,\frac{{0.25}}{{30}}\)
\(\frac{1}{2}\, \times \frac{{ - \,\Delta \,[{N_2}{O_5}]}}{{\Delta t}}\, = \frac{1}{4}\, \times \frac{{ - \,\Delta \,[N{O_2}]}}{{\Delta t}}\)
\(\frac{{\Delta \,[N{O_2}]}}{{\Delta t}}\, = \,\frac{{0.25}}{{30}}\, \times \,2\, = \,1.66\, \times \,{10^{ - 2}}\,M/\min \)
Download our appand get started for free
Similar Questions
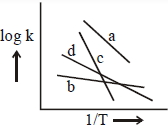
- 1ચાર જુદી જુદી પ્રક્રિયાઓ માટે વેગ અચળાંક વિરુદ્ધ $\frac{1}{\mathrm{T}}$ ના નીચેના આલેખ ધ્યાનમાં લો. તો આ પ્રક્રિયાઓની સક્રિયકરણ ઊર્જાઓ માટે નીચેના પૈકી ક્યો ક્રમ સાચો છે ?View Solution
- 2પ્રક્રિયાઓ $M, N,O$ અને $P$ માટે સક્રિયકરણ ઊર્જાનો કમ અનુક્રમે $E_M < E_N < E_O < E_P$ છે. તો કઇ પ્રક્રિયા માટે $K_{310}/K_{300}$ મહતમ થશે ?View Solution
- 3View Solutionનીચેનામાંથી કયો આલેખ સક્રિયકરણ ઊર્જાનું મૂલ્ય આપણને આપે છે?
- 4View Solutionઓરડાના તાપમાને હાઇડ્રોજન અને ઓક્સિજનનુ મિશ્રણ ખૂબ સ્થાયી છે. પરંતુ સ્પાર્ક કરવાથી તરત જ વિસ્ફોટ થાય છે. કારણ કે .........
- 5આર્ગોનની હાજરીમાં $N_2O$ નુ $N_2$ અને $O_2$ માં વિઘટન પ્રથમ કમની ગતિકીને અનુસરે છે. $K = 5.0 \times10^{11}\,e^{-2000/T}$ હોય તો પ્રકીયા સક્રિયકરણ ઊર્જા થશે?View Solution
- 6નીચે બે વિધાન આપેલા છે :View Solution
વિધાન $I$ : $A+B \rightarrow C$ પ્રક્રિયા માટે વેગ નિયમ, વેગ $(r)=k[A]^2[B]$ છે. જ્યારે $A$ અને $B$ એમ બંને ની સાંદ્રતા બમણી કરવામાં આવે છે ત્યારે પ્રક્રિયા વેગ વધી ને " $x$ " ગણો થાય છે.
વિધાન $II$ :
(Image)
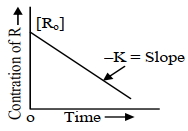
આકૃતિ " " $y$ " ક્રમ પ્રક્રિયા માટે સાંદ્રતામાં તફ઼ાવત સામે સમયનો આલેખ દર્શાંવે છે. $x+y$ નું મૂલ્ય . . . . . છે.
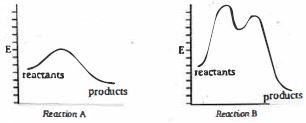
- 7View Solutionનીચેની બે પ્રક્રિયાઓ માટે, કયુ વિધાન સાચું છે?
- 8View Solutionજો સાંદ્રતા મોલ/લિટરમાં દર્શાવવામાં આવે તો પ્રથમક્રમની પ્રક્રિયા માટે વેગ અચળાંકનો એકમ........ છે.
- 9નીચે આપેલ માહિતી પરથી $H_2 + I_2\rightarrow 2HI$ પ્રક્રિયા માટે સક્રિયકરણ ઊર્જા .....View Solution
$T$ (in, $K$) $- 769$ , $1/T$ (in, $K^{-1}$ ) $- 1.3\times 10^{-3},$
$\log_{10}K - 2.9\,T$ (in, $K$) $- 667$, $1/T$ (in, $K^{-1}) - 1.5\times 10^{-3}$, $\log_{10}\,K - 1.1$
- 10પ્રથમ ક્રમની રાસાયણિક પ્રક્રિયાનો અર્ધઆયુ સમય $6.93$ મિનિટ છે. તો $99\%$ રાસાયણિક પ્રક્રિયા પૂર્ણ થવા માટે ........ મિનિટ જરૂરી છે. $(\log \,2 = 0.301)$View Solution
