Number of moles \(= \frac {1}{35.5}\)
Given, \(1\,eV = 23.06\,kcal\,mol^{-1}\)
\(3.7\,eV = 3.7 \times 23.06\,kcal\,mol^{-1}\)
i.e. \(1\) mole realease enegry
\(=3.7 \times 23.06\,kcal\)
\(\therefore \) Energy released
\(=\frac{1}{35.5}\times 3.7\times 23.06\,kcal=2.4\,kcal\)
Download our appand get started for free
Similar Questions
- 1$25^{\circ} C$ અને $1$ વાતા દબાણે દહન એન્થાલ્પીનો નીયે આપેલ છે.View Solution
પદાર્થ $H _{2}$ $C$(ગ્રેફાઈટ) $C _{2} H _{6}( g )$ $\frac{\Delta_{ C } H ^{\Theta}}{ kJmol ^{-1}}$ $-286.0$ $-394.0$ $-1560.0$ તો,ઈથેનની સર્જન એન્થાલ્પી ........
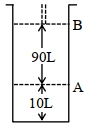
- 2આપેલ આક્રૂતિને ધ્યાનમાં લો.View Solution
$18^{\circ} \mathrm{C}$ પર, સ્થાન $A$ પર, પિસ્ટન સાથે જોડેલા (fitted) સિલિન્ડર માં આદર્શ વાયુનો $1$ $\mathrm{mol}$ રાખેલ છે. જો તાપમાન માં કોઈપણ જાતનો ફેરફાર ન કરીએ તો પિસ્ટન એ સ્થાન $B$ તરફ ખસે છે ત્યારે આ પ્રતિવર્તી પ્રક્રમ માં થયેલ કાર્ય $'x' L atm$ છે. $x=-$ ........... $L.atm$ (નજીક નો પૂર્ણાક)
[આપેલ : નિરપેક્ષ તાપમાન $={ }^{\circ} \mathrm{C}+273.15, \mathrm{R}=0.08206 \mathrm{~L} \mathrm{~atm} \mathrm{~mol}^{-1} \mathrm{~K}^{-1}$ ]
- 3સમાન તાપમાને $CH_4, C_2H_6, C_2H_4$ અને $C_2H_2$ વાયુઓની દહન ઉષ્મા અનુક્રમે $-212.8, -373.0, -337.0$ અને $-310.5\, Kcal$ છે. તો આ વાયુઓ પણ શ્રેષ્ઠ બળતણ કયું છે?View Solution
- 4$350\,K$ પર આદર્શ વાયુ અને $4\,atm$ થર્મલ વાહક દિવાલોના $2.0\,L$ પાત્રમાં હોય છે, જે પર્યાવરણના સંપર્કમાં હોય છે.તે $4\,atm$ ના અચળ દબાણ વિરુદ્ધ સમતાપી પ્રતિવર્તી $........\,J\,K ^{-1}$ છે.(નજીકનો પૂર્ણાક) આપેલ : $R =8.314\,J\,K ^{-1}\,mol ^{-1}$.View Solution
- 5$300\, K$ તાપમાને પર એક આદર્શ વાયુનો એક મોલ $1$ લિટરના પ્રારંભિક કદથી $10$ લિટર સુધીનો સમતાપી રીતે વિસ્તૃત થાય છે. આ પ્રક્રિયા માટે $\Delta E$નું મૂલ્ય છે $(R = 2\, cal\, mol^{-1}\, K^{-1})$View Solution
- 6View Solutionરાસાયણિક પ્રક્રિચાઓના નીચેની ક્યા જોડકા ચોક્કસપણે પ્રક્રિયાની સ્વયંભૂયિતા દર્શાવશે ?
- 7$2C_8H_{18}$$_{(g)}$ $+$ $25$$O_2$$_{(g)}$ $\rightarrow$ $16$$CO_2$$_{(g)}$ $+ 18$ $H_2O$$_{(g)}$ પ્રક્રિયા વાહનોમાં થાય છે. $\Delta H$, $\Delta S$ અને $\Delta G$ ની સંજ્ઞા શું થશે ?View Solution
- 8$0\,^oC$ એ $1 \,kg$ બરફનું ગલન દરમિયાન થતો એન્ટ્રોપી ફેરફાર $SI$ એકમમાં ગણો. બરફની ગલન ઉષ્મા = $80\, cal \,g^{-1}$ ....$JK^{-1} \,gm^{-1}$View Solution
- 9$Cl_2$$_{(g)}$ $\rightarrow$ $2Cl$$_{(g)}$, આ પ્રક્રિયામાં $\Delta$ $H$ નું મૂલ્ય .......View Solution
- 10નીચે આપેલ માહિતી પરથી $OH^-$ આયનની સર્જન-ઉષ્માની કીમત $252\,^oC$ તાપમાને.....$KJ$ શોધો.View Solution
${H_2}{O_{(l)}} \to \,\,H_{(aq)}^ + + \,\,OH_{(aq)}^ - \,;\,\,\,\Delta H\,\, = \,\,57.32\,\,KJ\,;$
${H_2}_{(g)} + \,\,\frac{1}{2}\,\,{O_2}_{(g)} \to \,\,{H_2}{O_{(1)}}\,;\,\,\Delta H\,\, = \,\, - 286.20\,\,KJ$
