$50\ mL$ $16.9\%$ $AgNO_3$ અને $50\ mL$ $5.8\%$ $NaCl$ના દ્રાવણને મિશ્ર કરતાં મળતાં અવક્ષેપનું વજન કેટલા .............. $\mathrm{g}$ હશે?
NEET 2015, Medium
b
Moles of $AgNO_3 =50 \times 16.9 / 100 \times 169.8$
Moles of $AgNO_3 =50 \times 16.9 / 100 \times 169.8$
$=0.05 \mathrm{mole}$
Moles of $\mathrm{NaCl}=50 \times 5.8 / 100 \times 58.5$
$=0.05 \mathrm{mole}$
$\mathrm{AgNO} 3+\mathrm{NaCl} \rightarrow \mathrm{AgCl}+\mathrm{NaNO} 3$
mass of $\mathrm{AgCl}=$ mole $\times$ molar mass
${=0.05 \times 143.5}$
${=7.16 \mathrm{g}}$
Download our appand get started for free
Experience the future of education. Simply download our apps or reach out to us for more information. Let's shape the future of learning together!No signup needed.*
Similar Questions
- 1$250\, {~mL}$ પાણીમાં $6.3\, {~g}$ ઓક્ઝેલિક એસિડ $\left({H}_{2} {C}_{2} {O}_{4} \cdot 2 {H}_{2} {O}\right)$ ઓગાળીને તૈયાર કરેલા દ્રાવણની મોલારિટી $\operatorname{mol} {L}^{-1}$ is ${x} \times 10^{-2}$ છે. ${x}$નું મૂલ્ય $.....$ છે. (નજીકના પૂર્ણાંકમાં)View Solution
[આણ્વિય દળ : ${H}: 1.0, {C}: 12.0, {O}: 16.0]$
- 2સમાન તાપમાને $10$ $dm^3$ જેટલા $N_2$ વાયુ અને $10$ $dm^3$ જેટલો $x$ વાયુ સમાન અણુઓ ધરાવે છે. તો તે $x$ વાયુ કયો હશે ?View Solution
- 3$120\,g$ એક કાર્બનિક સંયોજન જે ફક્ત કાર્બન અને હાઈડ્રોજન ધરાવે છે જ્યારે તેનું સંપૂર્ણ દહન કરવામાં આવે તો તે $330\,g\,\,CO _{2}$ અને $270\,g$ પાણી આપે છે. કાર્બન અને હાઈડ્રોજનની ટકાવારી અનુક્રમે શોધો.View Solution
- 4View Solutionનીચેનામાથી શેમાં મહત્તમ અણુઓ હશે?
- 5એક લંબઘન પદાર્થ છલોછલ $20$ લિટર પાણી ભરેલું છે. આ પદાર્થ ની લંબાઈ $30$ સેમી તેમજ પહોળાઇ $25 $ સેમી હોય, તો ઊચાઇ ..... ડેસીમીટર થાય.View Solution
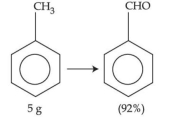
- 6ઉપરની પ્રક્રિયામાં $5\, g$ ટોલ્યુઈનનું $92\, \%$ સાથેના બેન્ઝાલ્ડીહાઈડ નીપજમાં પરિવર્તન થાય છે. ઉત્પન્ન થયેલ બેન્ઝાલ્ડીહાઈડનો જથ્થો $........\,\times 10^{-2}\, g$ છે. (નજીકના પૂર્ણાંકમાં)View Solution
- 7એક વાયુ જેનું સૂત્ર $(CO)_x$ છે. તેની બાષ્પ ઘનતા $70$ છે. તો $x$ નું મુલ્ય શું થાય ?View Solution
- 8કેટલા મોલ મેગ્નેશિયમ ફોસ્ફટ $Mg_3(PO_4)_2$ એ $0.25$ મોલ ઓક્સિજનના પરમાણુઓ ધરાવે ?View Solution
- 9વાયુની બાષ્પ ઘનતા $16$ છે. જો અચળ દબાણે વિશિષ્ટ ઉષ્મા અને અચળ કદ વિશિષ્ટ ઉષ્માનો ગુણોત્તર $1.4$ છે.તો તેનો પરમાણુ ભાર શોધો.View Solution
- 10કેલ્શિયમની પાણી સાથેની પ્રક્રિયા નીચે મુજબ છે:$Ca + 2H_2O \to Ca(OH)_2 + H_2$View Solution
$8\, gm$ કેલ્શિયમની પાણી સાથે $STP$ એ સંપૂર્ણ પ્રક્રિયા થાય ત્યારે કેટલા ............. $\mathrm{cm}^{-3}$ હાઈડ્રોજન ઉત્પન્ન થશે?
