$Mn^{2+} + 2e^- \rightarrow Mn,\, $$E^o = - 1.18\, V$
$Mn^{2+} \rightarrow Mn^{3+} + e^-,$ $ E^o = - 1.51 \,V$
તો પ્રક્યિા $3Mn^{2+} \rightarrow Mn^o + 2Mn^{3+},$ માટે $E^o$ તથા પુરોગામી પ્રક્રિયાની શક્યતા અનુક્રમે .... થશે.
\(\mathrm{Mn}^{2+}+2 \mathrm{e}^{-} \longrightarrow \mathrm{Mn}, \mathrm{E}^{\circ}=-1.18 \mathrm{V}\) .... \((i)\)
\(2\left(\mathrm{Mn}^{3+}+\mathrm{e}^{-} \longrightarrow \mathrm{Mn}^{2+}\right), E^{\circ}=+1.51 \mathrm{V}\).... \((ii)\)
Subtracting Eq. \((ii)\) from Eq. \((i)\), we get
\({3 \mathrm{Mn}^{2+} \longrightarrow \mathrm{Mn}+2 \mathrm{Mn}^{3+}}\)
\({E^{\circ}=-1.18-(+1.51)=-2.69 \mathrm{V}}\)
since, the value of \(E^{\circ}\) is -ve, therefore the reaction is non-spontaneous
Download our appand get started for free
Similar Questions
- 1$CaCl_2$ ના દ્રાવણમાંથી $25$ મિલિ ઍમ્પિયર વિદ્યુતપ્રવાહ $60 $ સેકન્ડ માટે પસાર કરતાં કેલ્શિયમના કેટલા પરમાણુ કૅથોડ પર જમા થશે ?View Solution
- 2પ્રમાણિત ધ્રુવ પોટેન્શિયલનું મૂલ્યનો ઉપયોગ કરી $I,\, II,\, III$ અને$ IV$ માંથી કયું વિધાન સાચું છે?View Solution
$Fe^{2+}_{(aq)} + 2e^{-} $$\rightleftharpoons$$ Fe_{(s)}$ ; $E^o = -0.44 \,V$,
$Cu^{2+}_{(aq)} + 2e^{-} $$\rightleftharpoons$$ Cu_{(s)}$ ; $E^o = + 0.34 \,V,$
$Ag^{+}(aq) + e^{-} $$\rightleftharpoons$$ Ag_{(s)}$ ; $E^o = + 0.80\,VI$
$I$ કોપરએ $FeSO_4$ દ્રાવણમાંથી આયર્ન દૂર કરે છે.
$II$. આયર્ન એ $CuSO_4 $ દ્રાવણમાંથી કોપર દૂર કરે છે.
$III.$ સિલ્વર એ $CuSO_4$ દ્રાવણમાંથી કોપર દૂર કરે છે.
$IV.$ આયર્ન એ $AgNO_3$ દ્રાવણમાંથી સિલ્વર દૂર કરે છે.
- 3ઝિંક સલ્ફેટના દ્રાવણમાં $40$ મિનિટ માટે $5$ એમ્પિ. પ્રવાહ પસાર કરવામાં આવે તો કેથોડ પર જમા થતું ઝીંક નું મૂલ્ય કેટલું થાય?View Solution
- 4$NaCl, HCl$ તથા $CH_3COONa$ ની અનંત મંદને મોલર - વાહકતા $(\Lambda ^o_m)$ અનુક્રમે $126.4, 425.9$ તથા $91.0\, S\, cm^2\, mol^{-1}$ છે. તો $CH_3COOH$ માટે $(\Lambda ^o_m)$ ........... $S\, cm^2 \,mol^{-1}$ થશે.View Solution
- 5પ્રક્રિયા $1/2 H_{2(g)} + AgCl_{(s)} \rightarrow H^{+}_{(aq)}.+ Cl^{-}_{(aq)} + Ag_{(s)}$ નીચેનામાંથી કયા ગેલ્વેનિક કોષમાં થાય છે?View Solution
- 6$ NaCl,\,KBr$ અને $ KCl$ માટે સીમાંત મોલર વાહકતા ${ \wedge ^0}$ અનુક્રમે $126,\,152 $ અને $150$ $S\ cm^2 \,mol^{ - 1}$ છે. તો $NaBr$ માટે ${ \wedge ^0}$ ......... ${\rm{S}}\,{\rm{c}}{{\rm{m}}^2}{\rm{mo}}{{\rm{l}}^{ - 1}}$ જણાવો.View Solution
- 7એક કોષ માટે, $Cu ( s ) \mid Cu ^{2+}\left(0.001 M || Ag ^{+}(0.01\,M ) \mid Ag ( s )\right.$View Solution
કોષ પોટિન્શયયલ $298 \,K$ એ $0.43\, V$ માલુમ પડ્યો, તો પ્રમાણિત ઇલેકટ્રોડ પોટિન્શયયલની માત્રા $Cu ^{2+} / Cu$ માટે $........\times 10^{-2} \,V \vartheta$ છે.
$[$ આપેલ છે $:E _{ Ag ^{+} / Ag }^{\Theta}=0.80\, V \text { and } \frac{2.303 \,RT }{ F }=0.06\,V ]$
- 8$2[Fe(CN)6]^{-3} + H_2O_2 + 2OH- \rightarrow 2[Fe(CN)_6]^{4-} + 2H_2O + O_2$ પ્રક્રિયામાં રીડકટન્ટનો તુલ્યભાર શું થશે ?$( Fe = 56, C = 12, N = 14, O = 16, H = 1)$View Solution
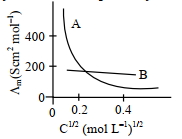
- 9વિધૂતવિભાજયો $A$ અને $B$ માટે મોલર વાહકતાઓ વિરુધ્ધ $C C1/2$ નો ગ્રાફ (આલેખ) નીચે દર્શાવેલ છે. વિધુતવિભાજ્યો $A$અને $B$ અનુક્રમે શોધો :View Solution
- 10જલીય $CuSO_4$ ના વિદ્યુત વિભાજનથી શું થાય?View Solution
