એનહાઈડ્રસ $CuSO_4$ અને $CuSO_4$.$5H_{2}O$ ની દ્રાવણ ઉષ્મા અનુક્રમે ${-1}5.89$ અને $2.80 \,K\,cal\, mol^{-1}$ છે. એનહાઈડ્રસ $CuSO_4$ ની હાઈડ્રેશન ઉષ્મા કેટલા .....$KCal$ હશે ?
Medium
a
નિર્બળ \(CuSO_4\) ની હાઈડ્રેશન ઉષ્મા \(=\) નિર્બળ ક્ષાર દ્રાવણની ઉષ્મા \(-\) હાઈડ્રેટ ક્ષારના દ્રાવણની ઉષ્મા
નિર્બળ \(CuSO_4\) ની હાઈડ્રેશન ઉષ્મા \(=\) નિર્બળ ક્ષાર દ્રાવણની ઉષ્મા \(-\) હાઈડ્રેટ ક્ષારના દ્રાવણની ઉષ્મા
\(= -15.89 - 2.80 = -18.69\, Kcal\)
Download our appand get started for free
Experience the future of education. Simply download our apps or reach out to us for more information. Let's shape the future of learning together!No signup needed.*
Similar Questions
- 1આપેલ આક્રૂતિને ધ્યાનમાં લો.View Solution
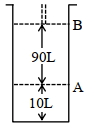
$18^{\circ} \mathrm{C}$ પર, સ્થાન $A$ પર, પિસ્ટન સાથે જોડેલા (fitted) સિલિન્ડર માં આદર્શ વાયુનો $1$ $\mathrm{mol}$ રાખેલ છે. જો તાપમાન માં કોઈપણ જાતનો ફેરફાર ન કરીએ તો પિસ્ટન એ સ્થાન $B$ તરફ ખસે છે ત્યારે આ પ્રતિવર્તી પ્રક્રમ માં થયેલ કાર્ય $'x' L atm$ છે. $x=-$ ........... $L.atm$ (નજીક નો પૂર્ણાક)
[આપેલ : નિરપેક્ષ તાપમાન $={ }^{\circ} \mathrm{C}+273.15, \mathrm{R}=0.08206 \mathrm{~L} \mathrm{~atm} \mathrm{~mol}^{-1} \mathrm{~K}^{-1}$ ]
- 2$1000\, K$ પર $CD_2O$ ની મોલર ઉષ્માક્ષમતા $(C_p)$ $10$ કેલરી છે. તો અચળ દબાણે $32\, g$ $CD_2O$ ને $1000\, K$ થી $100\, K$ તાપમાને ઠંડુ પાડવા સાથે સંકળાયેલ એન્ટ્રોપી ફેરફાર ....$cal\, deg^{-1}$. ($D\, =$ ડયુટેરિયમ, પરમાણ્વિય દળ $= 2\,u$ )View Solution
- 3સ્વયંભૂ પ્રક્રિયા માટે $\Delta G$ સંતુલન અચળાંક $(K)$ અને $E^o_{cell}$ શું થાય?View Solution
- 4$C{O_2}$ની સર્જન પ્રમાણિત મોલર એન્થાલ્પી ..... બરાબર છે.View Solution
- 5પ્રક્રિયા $2S{O_2}{\kern 1pt} (g)\, + \,{O_2}\,(g)\, \to \,2S{O_3}\,(g)$ માટેView Solution
${\Delta _H}\, = \, - 57.2\,kJ\,mo{l^{ - 1}}$ અને ${K_C} = 1.7\, \times \,{10^{16}}$ છે. નીચેના પૈકી ક્યુ વિધાન ખોટુ છે ?
- 6સંપૂર્ણ વાયુના નમૂના માટે જ્યારે તેના દબાણનો ફેરફાર સમોષ્મી રીતે $p_i$ થી $p_f,$ કરવામાં આવે છે ત્યારે એન્ટ્રોપી ફેરફાર નીચેનામાથી કઈ રીતે આપવામાં આવે છેView Solution
- 7ચુનાના પત્થરમાંથી ચુનાના રૂપાંતરણમાં,$CaCO_{3(s)} \rightarrow CaO_{(s)} + CO2_{(g)} 298 \,K$ અને $1$ બાર દબાણે $ \Delta H^°$ અને $ \Delta S^°$ ના મુલ્ય અનુક્રમે $+179.1\, kJ$ મોલ$^{-1}$ અને $160.2\, J/K$ છે. $ \Delta H^°$ અને $ \Delta S^°$ તાપમાન સાથે બદલાતા નથી. ઉપરના .....$K$ તાપમાને ચુનાના પત્થરથી ચુનાના રૂપાંતરણ સ્વયંભુ રીતે થશે ?View Solution
- 8$100\,^oC$ તાપમાને પ્રવાહી પાણીના બાષ્પમાં રૂપાંતર સાથે સંકળાયેલ એન્થાલ્પી/ફેરફાર $40.8\, kJ\, mol^{-1}$ છે. તો આ પ્રકમ માટે એન્ટ્રોપી ફેરફાર ....$J\,{K^{ - 1}}\,mo{l^{ - 1}}$ થશે.View Solution
- 9પ્રતિવર્તીં પ્રક્રિયા માટે $T = 300\,K,$ કદ વધીને $V_f = 1\,L$ થી$ V_f = 10\,L$ થાય છે. તો જો પ્રક્રિયા સમઉષ્મીય હોય તો $\Delta H$ ................. $\mathrm{kJ}$ શોધો.View Solution
- 10$300\, K$ તાપમાને એક મોલ આદર્શ વાયુ $2\,L$ કદમાંથી $6\,L$ કદમાં સમતાપી વિસ્તરણ કરવામાં આવે છે. તો આ પ્રકમ માટે $\Delta U$ ............. થશે.View Solution
