\(C + O_2 → CO_2 : \Delta H = -94.3\)
કિલોકેલેરી,
\(C + \frac{1}{2}{O_2} \to CO\,:\,\,\,\Delta H\,\, = \,\, - 26\) કિલોકેલેરી
આને સર્જન એન્થાલ્પી પણ કહે છે.
દહન એન્થાલ્પી માટે \(1\) મોલ કાર્બનિક સંયોજનનું સંપૂર્ણ દહન થવું જાઈએ
\(C + O_2 → CO_2\)
પ્રક્રિયામાં એક મોલ કાર્બનનું સંપૂર્ણ દહન થાય છે
\(C\) ની દહન એન્થાલ્પી = \(-94.3\) કિલોકેલરી થાય.
Download our appand get started for free
Similar Questions
- 1$273\, K$ એ પ્રક્રિયા એન્થાલ્પી $-3.57 \,KJ$ છે. જો $\Delta$$CP$ = શૂન્ય હોય તો $373\, K$ એ પ્રક્રિયાની એન્થાલ્પી કેટલી થશે ?View Solution
- 2આપેલ આકૃતિના આધારે, સાયા વિધાન/નો ની સંખ્યા $.........$ છે.View Solution
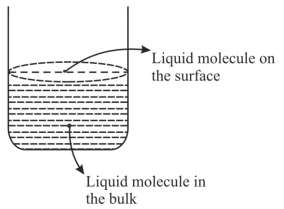
$A.$ જથ્થામાં (બલ્કમાં) પ્રવાહી અણુ પર આકર્ષણ અને અપાકર્ષણ બળો સમાન રીતે વર્તે ત્યારે પૃષ્ઠતાણનું નિર્માણ થાય છે.
$B.$ સપાટી ઉપર હાજર અણુઓ પર અસમાન બળો પ્રવર્તમાન $(uneven\,forces)$ના કારણે પૃષ્ઠતાણ છે.
$C.$ જથ્થામાં (બલ્કમાં) અણુ પ્રવાહી સપાટી (સ્તર) પર આવતાં નથી.
$D.$ જો પ્રણાલી એ બંધ પ્રણાલી હોય તો સપાટી ઉપરના અણુઓ એ બાષ્પદબાણ માટે જવાબદાર છે.
- 3$4NO_2$$_{(g)}$ $+$ $O_2$$_{(g)}$ $\rightarrow$ $2N_2O_5$$_{(g)}$, $\Delta_rH$ $= -111$ $KJ$. પ્રક્રિયાને ધ્યાનમાં લેતા ઉપરની પ્રક્રિયામાં જો $N_2O_5$$_{(s)}$ એ $N_2O_5$$_{(g)}$ ના બદલે બને તો $\Delta_rH$ નું મૂલ્ય ......$kJ$ થશે ? ($N_2O_5$ માટે ઉધ્વપતિનનું $\Delta H = 54\, kJ\, mol^{-1}$ આપેલું છે.)View Solution
- 4$NaOH$$_{(aq)}$ $+ HCl$$_{(aq)}$ $\rightarrow$ $NaCl$$_{(aq)}$ $+ H_2O$ $_{(aq)}$, એન્થાલ્પી ફેરફારને શું કહે છે ?View Solution
- 5કોષમાં થતી પ્રક્રિયા માટે.View Solution
$Pt ( s )\left| H _{2}( g )\right| H ^{+}( aq ) \| Ag ^{+}( aq ) \mid Ag ( s )$
$E _{\text {Cell }}^{0}=+0.5332 \,V$.
$\Delta_{ f } G ^{0}$ નું મૂલ્ય..........$k\,J\, mol ^{-1}$ છે. (નજીકનો પૂર્ણાંક)
- 6$\mathrm{A}(l) \rightarrow 2 \mathrm{B}(\mathrm{g})$ પ્રક્રિયા માટે $300\; \mathrm{K}$ પર $\Delta \mathrm{U}=2.1\; \mathrm{kcal}, \Delta \mathrm{S}=20\; \mathrm{cal} \mathrm{K}^{-1}$ છે. તો $\Delta \mathrm{G}$ માં $\mathrm{kcal}$... થશે.View Solution
- 7$25^{\circ} C$ અને $1$ વાતાવરણે નીચેનામાંથી કોની એન્ટ્રોપીનું મૂલ્ય સૌથી વધુ હશે ?View Solution
- 8બોમ્બ કેલેરીમીટરમાં એક મોલ ઝીંક રજ સાથે એક મોલ સલ્ફયુરીક એસિડની ઉષ્માક્ષેપક પ્રક્રિયા માટે $\Delta U$ અને $w$ નો સંબંધ .....View Solution
- 9View Solutionનીચેના પૈકી ક્યુ સાચું છે ?
- 10View Solutionજો પ્રક્રિયા...... હોય તો પ્રણાલી અને તેનાં વાતાવરણ માટે કુલ એન્ટ્રોપીનો ફેરફારમાં વધારો થાય છે.
