$2MnO_4^ - + 10{I^ - } + 16{H^ + } \to 2M{n^{2 + }} + 5{I_2} + 8{H_2}O$ તો $I_2$ ના ઉત્પન્ન થવાનો દર......$\times {10^{ - 2}}\,M{s^{ - 1}}$ જણાવો
Given \( - \,\frac{{dMnO_4^ - }}{{dt}}\, = \,4.56\, \times {10^{ - 3}}\,M{s^{ - 1}}\)
From the reaction given,
\( - \frac{1}{2}\,\frac{{dMnO_4^ - }}{{dt}}\, = \,\frac{{4.56 \times {{10}^{ - 3}}}}{2}\,M{s^{ - 1}}\)
\( - \frac{1}{2}\,\frac{{dMnO_4^ - }}{{dt}}\, = \,\frac{1}{5}\,\frac{{d{I_2}}}{{dt}}\)
\(\therefore \,\, - \frac{5}{2}\,\frac{{dMnO_4^ - }}{{dt}}\,\, = \frac{{d{I_2}}}{{dt}}\)
On substituting the given value
\(\therefore \frac{{d{I_2}}}{{dt}}\, = \,\frac{{4.56\, \times {{10}^{ - 3}} \times 5}}{2}\, = \,1.14\, \times \,{10^{ - 2}}\,M/s\)
Download our appand get started for free
Similar Questions
- 1$25\,^oC$ તાપમાને એક પ્રક્રિયાનો વેગ અચળાંક $1 \times 10^{-3}\,s^{-1}$ છે. જો તાપમાન વધારીને $35\,^oC$ કરતા પ્રક્રિયાનો વેગ બમણો થતો હોય, તો આ પ્રક્રિયાની સક્રિયકરણ ઊર્જા .......... $kJ\, mol^{-1}$ થશે.View Solution
- 2એક પ્રથમ ક્રમની પ્રક્રિયાતો અર્ધઆયુષ્ય સમય $15$ મિનિટ છે. તો એક ક્લાક પછી પદાર્થનો કેટલો જથ્થો બાકી રહેશે ?View Solution
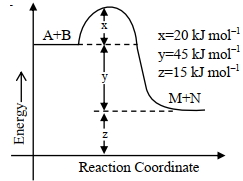
- 3નીચેના આંકડા મુજબ, પ્રક્રિયાના એન્થાલ્પી ફેરફારની તીવ્રતાView Solution
${A}+{B} \rightarrow {M}+{N}$ $......$ ${kJ} {mol}^{-1}$ બરાબર છે. (નજીકના પૂર્ણાંકમાં)
- 4પ્રથમ ક્રમ પ્રક્રિયા માટે, $75 \,\%$ પૂર્ણ થવા માટેનો સમય અને $50\, \%$ પૂર્ણ થવા માટેનો સમયનો ગુણોત્તર $....$ છે. (પૂર્ણાંકમાં જવાબ)View Solution
- 5રાસાયણિક પ્રક્રિયા $A \rightarrow B$ માટે પુરોગામી દિશામાં સક્રિયકરણ ઉર્જા $Ea$ છે. તો પ્રતિગ્રામી દિશામાં સક્રિયકરણ ઉર્જા.........View Solution
- 6પ્રથમ ક્રમની એક પ્રકિયા $15\,\min$ માં $75\%$ પૂર્ણ થાય, તો પ્રક્રિયાને $90\%$ પૂર્ણ થતા ........... $\min$ લાગશે.View Solution
- 7View Solutionપ્રદિપ્તીનુ બુઝાવુ ........ પર આધાર રાખે છે.
- 8$2 \mathrm{~A}+\mathrm{B} \rightarrow \mathrm{C}+\mathrm{D}$ પ્રક્રિયા ના ગતિકીય અભ્યાસ દરમિયાન, નીચે મુજબ ના પરિણામો પ્રાપ્ત થયા.View Solution
$A[M]$ $B[M]$ સર્જન નો પ્રારંભિક વેગ $D$
$i$ $0.1$ $0.1$ $6.0 \times 10^{-3}$ $ii$ $0.3$ $0.2$ $7.2 \times 10^{-2}$ $ii$ $0.3$ $0.4$ $2.88 \times 10^{-1}$ $iv$ $0.4$ $0.1$ $2.40 \times 10^{-2}$ ઉપ૨ની માહિતી ના આધારે સમગ્ર પ્રક્રિયાનો ક્રમ ........ છે.
- 9ઓરડાના તાપમાને $NO$ અને $O_2$વચ્ચે પ્રક્રિયા થઈ $NO_2$ મળે જે ઝડપી થાય છે. જ્યારે $CO $ અને $O_2$ વચ્ચે પ્રક્રિયા ધીમી થાય કારણ કે.....View Solution
- 10પ્રક્રિયા $ : A $ $\rightleftharpoons$ $ B$ માં $Ea$ પુરોગામી પ્રક્રિયાની સક્રિયકરણ ઊર્જા છે. તો પ્રતિગામી પ્રક્રિયાની સક્રિયકરણ ઊર્જા......View Solution
