Question Bank
Explore our large set of questions to practice for your standard seamlessly- 1$4.0\,L$ એક આદર્શ વાયુને શૂન્યાવકાશમાં જ્યાં સુધી તેનું કુલ કદ $20\,L$ ન થાય ત્યાં સુધી સમતાપીય રીતે વિસ્તરણ પામવા દેવામાં આવે છે તો આ વિસ્તરણમાં શોષાતી ઉષ્માનો જથ્થો $.....\,L\,atm$ છે.View Solution
- 2અચળ કદ કેલોરીમીટરમાં એક વાયુ (મોલર દળ $=280\, g\, mol ^{-1}$ ) ને વધુ $O _2$ માં સળગાવવામાં આવ્યો અને દહન દરમયાન કેલોરીમીટરનું તાપમાન $298.0\, K$ થી $298.45\, K$ વધે છે. જો કેલોરીમીટરની ઉષ્માક્ષમતા $2.5\, kJ\,K -1$ અને વાયુની દહન એન્થાલ્પી $9\, kJ \,mol ^{-1}$ હોય તો પછી $.....\,g$ વાયુનો જથ્થો સળગ્યો હોવો જોઈએ. (નજીકનો પૂર્ણાંક)View Solution
- 3અચળ દબાણો, આદર્શ વાયુની મોલર ઉષ્માક્ષારતા $20.785 \,JK ^{-1} mol ^{-1}$ છે. તેને $300 \,K$ થી $500 \,K$ તાપમાને ગરમ કરતા આંતરિક ઊર્જામાં થતી ફેરાર $5000 \,J$ છે. તો અચળકદે વાયુના મોલની સંખ્યા ........... છે. (નજીકનો પૂણાઈં) (આપેલું છે: $R=8.314 \,J K ^{-1} mol ^{-1}$ )View Solution
- 4કોષમાં થતી પ્રક્રિયા માટે.View Solution
$Pt ( s )\left| H _{2}( g )\right| H ^{+}( aq ) \| Ag ^{+}( aq ) \mid Ag ( s )$
$E _{\text {Cell }}^{0}=+0.5332 \,V$.
$\Delta_{ f } G ^{0}$ નું મૂલ્ય..........$k\,J\, mol ^{-1}$ છે. (નજીકનો પૂર્ણાંક)
- 5View Solutionનીચે આપેલા સંબંધો માંથી ક્યો સાચો નથી ?
- 6પ્રોપેન, ગ્રેફાઈટ અને ડાયહાઈડ્રોજનની $298 \,K$ એ દહન એન્થાલ્પી અનુક્રમે, $-2220.0 \,kJ \,mol ^{-1},-393.5 \,kJ\,mol ^{-1}$ અને $-285.8 \,kJ\, mol ^{-1}$ છે. તો પ્રોપેન $\left( C _3 H _8\right)$ ની સર્જન એન્થાલ્પીની માત્રા $......\,kJ \,mol ^{-1}$ (નજીકનો પૂર્ણાંક)View Solution
- 7મિથેનોલનું સંપૂર્ણ દહન માટે,View Solution
$CH _{3} OH (1)+\frac{3}{2} O _{2}( g ) \rightarrow CO _{2}( g )+2 H _{2} O (1)$
$27^{\circ} C$ પર ઉત્પન્ન થતી ઉષ્માનો જથ્થો બોમ્બ કેલોરિમીટર વડે માપતા $726\,kJ\,mol ^{-1}$ મળે છે.પ્રક્રિયા માટે દહન એન્થાલ્પી $-x$ છે જ્યાં $x\,\,\dots\dots\dots$ $kJ\,mol^{-1}$ છે.(નજીકનો પૂર્ણાંક)
(આપેલ $: R =8.3\, J\,K ^{-1} \,mol ^{-1}$ )
- 8મિસેલ બનાવટ માટે નીચે આપેલા વિધાનોમાંથી કયું સાચુ છે ?View Solution
$A.$ મિસેલ બનાવટ એ એક ઉષ્માક્ષેપક પ્રક્રમ છે.
$B.$ મિસેલ બનાવટ એ એક ઉષ્માશોષક પ્રક્રમ છે.
$C.$ એન્ટ્રોપી ફેરફાર ધન છે.
$D$ એન્ટ્રોપી ફેરફાર ઋણ છે.
- 9સૂચી $-I$ ને સૂચી $-II$ સાથે જોડો.View Solution
સૂચી$-I$ સૂચી$-II$ $(A)$ સ્વયંસ્ફુરિત પ્રક્રમ $(I)\,\Delta H < 0$ $(B)\,\Delta P =0\;\Delta T =0$ સાથે પ્રક્રમ $(II)\,\Delta G _{ T , P } < 0$ $(C)\,\Delta H _{reaction}$ $(III)$ સમતાપિય અને સમદાબીય પ્રક્રિયા $(D)$ ઉષ્માક્ષેપક પ્રક્રિયા $(IV)$ [પક્રિયક અણુની બંધ ઉર્જાઓ] - [નીપજ અણુંની બંધ ઉર્જાઓ] નીચે આપેલ વિકલ્પમાંથી યોગ્ય ઉત્તર પસંદ કરો.
- 10ઉષ્માગતિકીય પ્રયોગ જ્યારે કરતા હોય ત્યારે એક વિદ્યાર્થીએ નીચે પ્રમાણે અવલોકનો મેળવ્યા.View Solution
$HCl + NaOH \rightarrow NaCl + H _{2} O \Delta H =-57.3\, kJ\,mol ^{-1}$
$CH _{3} COOH + NaOH \rightarrow CH _{3} COONa + H _{2} O$
$\Delta H =-55.3\,kJ\,mol ^{-1}$
વિદ્યાર્થી દ્વારા ગણતરી કરેલ $CH_3COOH$ની આયનિકરણ એન્થાલ્પી $......\,kJ\, mol ^{-1}$ છે.
- 11એક માછલી એક પાણી સંગ્રહ $(water\,body)$માં તરતી હતી. જ્યારે તેને એકદમ જ પાણી સંગ્રહમાંથી બહાર કાઢવામાં આવી ત્યારે તેના ઉપર પાણીની ફિલ્મ સાથેના આવરણ, તેનું વજન $36\,g$ છે. જ્યારે તેને $100^{0}C$ ઉપર રાંધવામાં આવે ત્યારે બાષ્પીભવનની આંતરિક ઊર્જા $.....\,kJ\,mol ^{-1}$ માં શોધો. [નજીકનો પૂર્ણાંક] [આપેલ : $373\,K$ અને $1\,bar$ પર પાણી માટે $\Delta_{ vap } H ^{\ominus}$ બાષ્પ $=41.1\,kJ\,mol ; R=8.31\,J$View Solution
- 12નીચેના પૈકી, અવસ્થા વિધયો સંખ્યા $....$ છે.View Solution
આંતરિક ઉર્જા $(U)$; કદ $(V)$; ઉષ્મા $(q)$; એન્થાલ્પી $( H )$
- 13$2.2\,g$ નાઈટ્રસ ઓકસાઇડ $\left( N _{2} O \right)$ ને $1\,atm$ ના અચળ દબાાણે અને $310\,K$ થી $270\,K$ સુધી ઠંડો કરવામાં આવે છે. કોઈ કારણે વાયુ $217.1\,ml$ થી $167.75\,ml$ સુધી દબાય છે. પ્રક્રમમાં આંતરીક ઊર્જામાં થતો ફેરફાર $\Delta U$ એ $-'x'\,J$ છે. તો $'x'$ નું મૂલ્ય $\dots\dots$ શોધો. [નજીકના પૂર્ણાંકમાં]View Solution
મોલર ઉષ્મા ક્ષમતા $N _{2} O\,100\,J\,K ^{-1}\,mol\,^{-1}$ )
- 14$298\, K$ અને $1 \,atm$ દબાણ પર $2.4\, g$ કોલસાને વધુ માત્રામાં ઓક્સિજન સાથે બોમ્બ કેલોરિમીટરમાં સળગાવવામાં આવે છે. કેલોરિમીટરનું તાપમાન $298 \,K$ થી $300 \,K$ વધે છે. કોલસાના દહન દરમિયાન એન્થાલ્પી ફેરફાર $-x\, kJ\, mol ^{-1}$ છે. તો $x$ નું મુલ્ય $.....$ છે. (નજીકનો પૂર્ણાંક)View Solution
(આપેલ : બોમ્બ કેલોરિમીટરની ઉષ્માક્ષમતા $20.0\, kJ/K.$ ધારી લો કે કોલસો એ શુધ્ધ કાર્બન છે.)
- 15એક પ્રક્રિયા માટે,View Solution
$H _{2} F _{2( g )} \rightarrow H _{2( g )}+ F _{2( g )}$
$\Delta U =-59.6\,kJ\,mol ^{-1}$ $27^{\circ}\,C$ પર,
ઉપરની પ્રક્રિયામાં એન્થાલ્પીમાં થતો ફેરફાર $(-)......\,kJ\, mol ^{-1}$ [નજીકનો પૂર્ણાંક]
(આપેલ : $\left.R =8.314 \,J\, K ^{-1} \,mol ^{-1}\right)$
- 16$C ( s )+ O _{2}( g ) \rightarrow CO _{2}( g )+400\; kJ$View Solution
$C ( s )+\frac{1}{2} O _{2}( g ) \rightarrow CO ( g )+100 \;kJ$
જ્યારે $60\,\%$ શુદ્ધતા ધરાવતા કોલસાને અપૂરતા ઓકિસજનની હાજરીમાં દહ્ કરતા, $60 \%$ કાર્બન $'CO'$માં અને બાકી રહેલો $'CO _2'$માં રૂપાંતર પામે છે. જ્યારે $0.6 \,kg$ કોલસાને બાળવામાં આવે ત્યારે ઉત્પન્ન થયેલી ઉષ્મા $......$
- 17જયારે $600\, mL \,0.2\, M \,HNO _3$ ને $400\, mL\, 0.1 \,M \,NaOH$ ના દ્રાવણ સાથે મિશ્ર કરવામાં આવે છે ત્યારે ફલાસ્કના તાપમાનમાં થતો વધારો $.......\times 10^{-2}{ }^{\circ} C$ છે.View Solution
(તટસ્થીકરણ એન્થાલ્પી $=57\, kJ \,mol ^{-1}$ અને પાણીની વિશિષ્ટ ઉષ્મા= $4.2 \,J\,K ^{-1} \,g ^{-1}$ )
- 18$2 {NO}_{2}({~g}) \rightleftharpoons {N}_{2} {O}_{4}({~g})$ પ્રક્રિયા માટે, જ્યારે $\Delta {S}=-176.0\, {JK}^{-1}$ અને $\Delta {H}=-57.8\, {~kJ}\, {~mol}^{-1}$, $298\, \mathrm{~K}$ પર પ્રક્રિયા માટે $\Delta {G}$ની તીવ્રતા $......\,{kJ} {mol}^{-1} .$ (નજીકના પૂર્ણાંકમાં)View Solution
- 19$373 {~K}$ અને $1$ બાર દબાણ પર પાણી માટે $\Delta_{\text {vap }} {H}=41 {~kJ} {~mol}^{-1}$. માની લઈએ કે પાણીની વરાળ એક આદર્શ વાયુ છે જે પ્રવાહી પાણી કરતા ઘણો મોટો જથ્થો ધરાવે છે, પાણીના બાષ્પીભવન દરમિયાન આંતરિક ઊર્જામાં ફેરફાર $...... {kJ} {mol}^{-1}$ છે.View Solution
[ઉપયોગ : $\left.{R}=8.3 \,{~J} \,{~mol}^{-1}\, {~K}^{-1}\right]$
- 20$495\, K$ પર $A ( g ) \rightleftharpoons B ( g )$ પ્રક્રિયા માટે $\Delta_{ I } G ^{\circ}=-9.478\, kJ\, mol ^{-1}$View Solution
જો આપણે બંધ પાત્રમાં $495\, K$ પર એનાં $22$ મિલીમોલ્સથી પ્રક્રિયા શરૂ કરીએ, તો સંતુલન મિશ્રણ એ $B$ની માત્રા ........ મિલિમોલ છે.
$\left[ R =8.314 J mol ^{-1} K ^{-1} ; \ell n 10=2.303\right]$
- 21$Al _{2} O _{3}$ અને $CaO$ બનવાની પ્રમાણિત એન્થાલ્પી અનુક્રમે $-1675\, kJ\, mol ^{-1}$ અને $-635\, kJ\, mol ^{-1}$ છે.View Solution
પ્રક્રિયા $3 CaO +2 Al \rightarrow 3 Ca + Al _{2} O _{3}$ માટે પ્રમાણિત પ્રક્રિયા એન્થાલ્પી $\Delta_{ r } H ^{0=}$ .......... $kJ$
- 22${KCl}$ માટે બોર્ન-હેબર ચક્રનું મૂલ્યાંકન નીચેની માહિતી સાથે કરવામાં આવે છે:View Solution
$\Delta_{f} {H}^{\ominus}$ ${KCl}=-436.7 \,{~kJ}\, {~mol}^{-1}$
$\Delta_{\text {sub }} {H}^{\ominus}$ ${K}=89.2 \,{~kJ}\, {~mol}^{-1}$
$\Delta_{\text {ionization }} \,{H}^{-}$ ${K}=419.0\, {~kJ}\, {~mol}^{-1}$
$\Delta_{\text {electron gain }} {H}^{\ominus}$ ${Cl}_{(\text {e) }}=-348.6 \,{~kJ} \,{~mol}^{-1}$
$\Delta_{{bond}} {H}^{-}$ ${Cl}_{2}=243.0 \,{~kJ} \,{~mol}^{-1}$
${KCl}$ની લેટિસ એન્થાલ્પીની તીવ્રતા $.....$ ${kJ} {mol}^{-1}$ છે.
- 23$Na _{( g )}$ માંથી $Na ^{+}$ ઉત્પન્ન થવાની આયનીકરણ એન્થાલ્પી $495.8\, kJ\, mol-1$ છે, જ્યારે $Br$ ની ઈલેક્ટ્રોન પ્રાપ્તિ એન્થાલ્પી $-325.0\, kJ\,mol^{-1}$ છે. $NaBr$ ની લેટાઈસ એન્થાલ્પી $-728.4\, kJ\, mol^{-1}$ આપેલ છે. તો આયોનીક ઘન $NaBr$ ની સર્જનમાટેની ઊર્જા $(-)$ ......... $\times 10^{-1} ,kJ \,mol ^{-1}$ છેView Solution
- 24$2 Fe ^{3+}( aq )+2 I ^{-}( aq ) \rightarrow 2 Fe ^{2+}( aq )+ I _{2}( s )$ પ્રકિયા પ્રમાણભૂત મુક્ત ઊર્જા પરિવર્તનની તીવ્રતા , $\Delta_{ r } G _{ m }^{\circ}=- ........... kJ$View Solution
$\left[ E _{ Fe ^{2+} / Fe ( s )}^{ o }=-0.440 V ; E _{ Fe ^{3+} / Fe ( s )}^{\circ}=-0.036 V\ E _{ I _{2} / 2 I ^{-}}^{ o }=0.539 V ; F =96500\, C \right]$ - 25એક પ્રણાલી $200\,J$ કાર્ય કરે છે અને તે જ સમયે $150 \,{~J}$ ગરમી શોષી લે છે. આંતરિક ઊર્જામાં ફેરફારની તીવ્રતા $..... \, J$ છે. (નજીકના પૂર્ણાંકમાં)View Solution
- 26નીચેની પ્રક્રિયાઓમાંથી જે દરમિયાન, એન્ટ્રોપી ઓછી થાય છે?View Solution
$(A)$ $0^{\circ} C$ પાણી નું બરફ બનવું
$(B)$ $-10^{\circ} C$ પાણી નું બરફ બનવું
$(C)$ $N _{2}( g )+3 H _{2}( g ) \rightarrow 2 NH _{3}( g )$
$(D)$ $CO ( g )$ નું શોષણ અને લેડ ની સપાટી
$(E)$ $NaCl$ નું પાણી માં ઓગાળવું
- 27પ્રક્રિયા માટેView Solution
$C _{2} H _{6} \rightarrow C _{2} H _{4}+ H _{2}$
પ્રકિયા એન્થાલ્પી $\Delta_{ r } H =...........{ kJ\, mol ^{-1}}$.
[આપેલ : બંધ એન્થાલ્પી $kJ$ $mol$ $^{-1}:C-C : 347, C = C : 611 ; C - H : 414, H - H : 436]$
- 28વ્યક્તિને દરરોજ સરેરાશ આશરે $10000\, {~kJ}$ ઊર્જાની જરૂર પડે છે. આ ઉર્જા જરૂરિયાતને પહોંચી વળવા માટે જરૂરી ગ્લુકોઝ $($મોલર દળ $=180.0\, {~g} \,{~mol}^{-1}$ ) $..... \, {g}$ છે. (નજીકનો પૂર્ણાંક)View Solution
(ઉપયોગ કરો : $\Delta_{{c}} {H}($ ગ્લુકોઝ $)=-2700\, {~kJ}\, {~mol}^{-1}$ )
- 29$200\, {~mL}$ $0.2\, {M} {HCl}$ એ $300\, {~mL}$ $0.1\, {M} {NaOH}$ સાથે મિશ્રિત છે. આ પ્રક્રિયાને તટસ્થ કરવાની મોલર ઉષ્મા $-57.1 \,{~kJ}$ છે. મિશ્ર કરતાં પ્રણાલીમાં તાપમાનમાં વધારો ${ }^{\circ} {C}$માં ${x} \times 10^{-2}$ છે. ${x}$નું મૂલ્ય $.....$ છે.View Solution
[આપેલ છે : પાણીની વિશિષ્ટ ઉષ્મા $=4.18\, {~J} \,{~g}^{-1}\, {~K}^{-1},$ પાણીની ઘનતા $=1.00\, {~g}\, {~cm}^{-3}$ ]
(ધારો કે મિશ્રણ પર કોઈ વોલ્યુમ ફેરફાર નથી)
- 30એક બોમ્બ કેલોરીમીટરમાં, સાયનામાઈડ $NH _{2} CN _{( s )}$ અને ઓકિસજનની પ્રક્રિયા કરવામાં આવે છે અને તેનો $\Delta U -742.24\, kJ\, mol ^{-1}$ માલૂમ પડયો. તો આપેલી પ્રક્રિયા માટે,View Solution
$NH _{2} CN _{( s )}+\frac{3}{2} O _{2}( g ) \rightarrow N _{2( g )}+ O _{2}( g )+ H _{2} O _{(l)}$
$\Delta H _{298}$ ની માત્રા ........ $kJ$ છે. (નજીક પૂર્ણાંક રાઉન્ડ ઓફ)
[ધારી લો આદર્શ વાયુઓ અને $\left. R =8.314\, J\, mol ^{-1} K ^{-1}\right]$
- 31એક રાસાયણિક પ્રક્રિયા $A+B \rightleftharpoons C+D$ માટે, $\left(\Delta_{ r } H ^{\Theta}=80\, kJ\, mol ^{-1}\right)$ એન્ટ્રોપીમાં થતો ફેરફાર $\Delta_{ r } S ^{\Theta}$ એ તાપમાન $T (K$ માં) પર આધારિત છે જે $\Delta_{ r } S^{\Theta}=2 T \left( J K ^{-1} mol ^{-1}\right)$ તરીકે છે.View Solution
કયા ન્યૂન્નતમ તાપમાને તે સ્વયંભૂ (આપ મેળે) થશે તે ............ $K$ માં છે. (પૂર્ણાક)
- 32નીચેની કોષની પ્રક્રિયા ધ્યાનમાં લો:View Solution
$\mathrm{Cd}_{(s)}+\mathrm{Hg}_{2} \mathrm{SO}_{4(s)}+\frac{9}{5} \mathrm{H}_{2} \mathrm{O}_{(l)} \rightleftharpoons \mathrm{CdSO}_{4} \cdot \frac{9}{5} \mathrm{H}_{2} \mathrm{O}_{(s)}+2 \mathrm{Hg}_{(l)}$
$25^{\circ} {C}$ પર ${E}_{\text {cell }}^{0}$નું મૂલ્ય $4.315\, {~V}$ છે.
જો $\Delta {H}^{\circ}=-825.2\, {~kJ} \,{~mol}^{-1}$, પ્રમાણિત એન્ટ્રોપી ફેરફાર $\Delta {S}^{\circ}$ ${J} \,{K}^{-1}$માં $........$ છે. (નજીકના પૂર્ણાંકમાં) [આપેલ: ફેરાડે અચળાંક $ = 96487 \, {C} \, {mol}^{-1} $]
- 33નીચેની પ્રક્રિયા માટે આપેલ માહિતી નીચે મુજબ છે:View Solution
${FeO}_{(0)}+{C}_{\text {(gaplike) }} \longrightarrow {Fe}_{(0)}+{CO}_{({g})}$
પદાર્થ $\Delta {H}^{\circ}$
$\left({kJ} {mol}^{-1}\right)$
$\Delta {S}^{\circ}$
$\left({J} {mol}^{-1} {~K}^{-1}\right)$
${FeO}_{(s)}$ $-266.3$ $57.49$ ${C}_{\text {(graphite) }}$ $0$ $5.74$ ${Fe}_{(s)}$ $0$ $27.28$ ${CO}_{({g})}$ $-110.5$ $197.6$ ${K}$માં લઘુત્તમ તાપમાન કે જેના પર પ્રક્રિયા સ્વયંભૂ બને છે તે $.......$ છે.(પૂર્ણાંકમાં જવાબ)
- 34$100^{\circ} {C}$ અને $1\, bar$એ પાણી માટેView Solution
$\Delta_{\text {vap }} {H}-\Delta_{\text {vap }} {U}=...... \times 10^{2} \,{~J}\, {~mol}^{-1}$.
$\left[\right.$ ઉપયોગ કરો : $\left.R=8.31\, {~J}\, {~mol}^{-1}\, {~K}^{-1}\right]$
[${H}_{2} {O}({l})$નું કદ ${H}_{2} {O}({g})$ના કદ કરતાં ઘણું નાનું ધારો. ધારો કે ${H}_{2} {O}({g})$ને આદર્શ વાયુ તરીકે ગણવામાં આવે છે]
- 35$25^{\circ} C$ પર, $50\, g$ આયર્ન સાથે $HCl$ ની પ્રક્રિયા થતાં $FeCl _{2}$ બનાવે છે. $1\, bar$ નાં અચળ દબાણે ઉત્પન્ન થતો હાઈડ્રોજન વાયુ વિસ્તરે છે. આ વિસ્તરણ દરમ્યાન વાયુ વડે થતું કાર્ય ..... $\,J$ છે. (નજીકનાં પૂર્ણાંકમાં રાઉન્ડ ઓફ કરો.).View Solution
[આપેલ : $R =8.314 \,J mol ^{-1} K ^{-1}$ ધારી લો કે હાઈડ્રોજન એ એક આદર્શ વાયુ છે.] [ પરમાણ્વીય દળ $Fe = 55.85\, u$ છે.]
- 36$298.2\, {~K}$ પર હાઇડ્રોજન $\left({E}_{{H}}\right)$ અને તેના આઇસોટોપ ડ્યુટેરિયમ $\left({E}_{{D}}\right)$ માટે બંધ વિયોજન એન્થાલ્પી (${kJ} \,{mol}^{-1}$ માં) નો સબંધ એ શ્રેષ્ઠ રીતે વર્ણવેલ છેView Solution
- 37$298\, {~K}$ પર ઘન $({X})$ના સંયોજનની એન્થાલ્પી $2.8 \,{k} {J}\, {mol}^{-1}$ અને પ્રવાહી $(X)$ બાષ્પીભવનની એન્થાલ્પી $98.2 \,{~kJ}\, {~mol}^{-1}$ છે.પદાર્થ $({X})$ની ઊર્ધ્વપાતનની એન્થાલ્પી $..... \,{kJ} \,{mol}^{-1}$ છે. (નજીકના પૂર્ણાંકમાં)View Solution
- 38$300\, {~K}$ પર આપેલ કેમિકલ $A \rightarrow B$ માટે મુક્ત ઊર્જા ફેરફાર $-49.4\, {~kJ} \,{~mol}^{-1}$ અને પ્રક્રિયાની એન્થાલ્પી $51.4\, {~kJ} \,{~mol}^{-1}$ છે. પ્રક્રિયાનો એન્ટ્રોપી ફેરફાર $.....\,{J}\, {K}^{-1}\, {~mol}^{-1}$ છે.View Solution
- 39આદર્શ વર્તણુંક ધારી લો, $25^{\circ} C$ પર નીચે આપેલ પ્રક્રિયા માટે $log\, K$ ની માત્રા $x \times 10^{-1}$ છે. તો $x$ નું મૂલ્ય ....... છે. (પૂર્ણાંકમાં જવાબ)View Solution
$3 HC \equiv CH _{( g )} \rightleftharpoons C _{6} H _{6(\ell)}$
[આપેલ : $\Delta_{f} G ^{\circ}( HC \equiv CH )=-2.04 \times 10^{5}\, J mol ^{-1}$
$\Delta_{f} G ^{\circ}\left( C _{6} H _{6}\right)=-1.24 \times 10^{5}\, J mol ^{-1} ; R =8.314\,\left. J K ^{-1} mol ^{-1}\right]$
- 40જ્યારે $400\, {~mL}$ $0.2\, {M} \,{H}_{2} {SO}_{4}$ દ્રાવણને $600\, {~mL}$ $0.1\, {M} \,{NaOH}$ દ્રાવણ સાથે મિશ્ર કરવામાં આવે છે, અંતિમ દ્રાવણના તાપમાનમાં થતો વધારો $....\,\times 10^{-2} \,{~K}$ છે.View Solution
$\left[\right.$ ઉપયોગ $: {H}^{+}({aq})+{OH}^{-}({aq}) \rightarrow {H}_{2} {O}: \Delta_{{\gamma}} {H}=-57.1\, {k} {J} \,{mol}^{-1},$
વિશિષ્ટ ઊર્જા ${H}_{2} {O}=4.18 {Jk}^{-} {g}^{-},$
ઘનતા ${H}_{2} {O}=1.0\, {~g} {~cm}^{-3},$
મિશ્રણ પર દ્રાવણના કદમાં કોઈ ફેરફાર થતો નથી એમ ધારો.]
- 41$1$ બાર અને $298\, K$ પર આદર્શ વાયુના પાંચ મોલને કદ બમણા કરવા માટે વેક્યૂમમાં વિસ્તૃત કર્યા છે. થયેલ કાર્ય:View Solution
- 42$25^{\circ} C$ એ એક ઓક્સિડેશન-રીડકશન પ્રક્રિયામાં ઇલેક્ટ્રોન્સનું સ્થાનાંતરણ થાય છે તેમાં $\Delta G ^{\circ}$ નું મૂલ્ય $17.37\, kJ$ $mol ^{-1}$ છે. તો $E _{\text {cell }}^{\circ}$ ($V$ માં) ........ $\times 10^{-2}$ થાય.View Solution
$\left(1 F =96,500\, C\, mol ^{-1}\right)$
- 43$NaCl$ દ્રાવણની લેટિસ એન્થાલ્પી અને એન્થાલ્પી અનુક્રમે $788\, kJ mol ^{-1}$ અને $4\, kJ\, mol ^{-1}$.$NaCl$ની જલીયકરણ એન્થાલ્પી.......$\, kJ\, mol ^{-1}$View Solution
- 44કેટલી આંતરિક ઉર્જા પરિવર્તન ($J$ માં) જ્યારે $90$ ગ્રામ પાણી $100^{\circ} C$ પર સંપૂર્ણ બાષ્પીભવન કરે છે ........View Solution
( $373\, K$ તાપમાને પાણી નું $\Delta H _{\text {vap }}$ $K =41$ કિલોજૂલ/મોલ $\left. R =8.314\, JK ^{-1} mol ^{-1}\right)$)
- 45આદર્શ વાયુના એક મોલ માટે, આમાંથી કયું વિધાન સાચું હોવું જોઈએ $?$View Solution
$(a)$ $U$ અને $H$ દરેક તાપમાન પર જ આધાર રાખે છે
$(b)$ દબનીયતા પરિબળ $z$ $1$ની બરાબર નથી
$(c)$ $C _{ P , m }- C _{ V , m }= R$
$(d)$ કોઈ પ્રક્રિયા માટે $d U = C _{ V } d T$
- 46View Solutionકઈ પ્રક્રિયા ઉષ્માશોષક પ્રક્રિયાનો સ્વભાવ ધરાવતી નથી :-
- 47ડાઇમરાઇઝેશન પ્રક્રિયા માટે,View Solution
$2 A ( g ) \rightarrow A _{2}( g )$
$298\, K$ પર $\Delta U^ \ominus,=-20\, kJ\, mol ^{-1}, \Delta S \odot=-30\, J$$K ^{-1}\, mol ^{-1},$ પછી $\Delta G ^{\ominus}$ ........$J$ હશે?
- 48View Solutionનીચેના વિધાનો પૈકી ક્યુ એક ડાલ્ટન દ્વારા આપવામાં આવ્યું ન હતું ?
- 49View Solutionનીચેની વચ્ચેનું સાચું વિધાન છે
- 50$\mathrm{A}(l) \rightarrow 2 \mathrm{B}(\mathrm{g})$ પ્રક્રિયા માટે $300\; \mathrm{K}$ પર $\Delta \mathrm{U}=2.1\; \mathrm{kcal}, \Delta \mathrm{S}=20\; \mathrm{cal} \mathrm{K}^{-1}$ છે. તો $\Delta \mathrm{G}$ માં $\mathrm{kcal}$... થશે.View Solution
- 51અચળ કહે, જ્યારે $4$ મોલ આદર્શ વાયુને $300\; \mathrm{K}$ થી $500\; \mathrm{K}$ સુધી ગરમ કરવામાં આવે ત્યારે તેની આંતરિક ઊર્જામાં $5000\; \mathrm{J}$ નો ફેરફાર થાય છે. તો અચળ કદ મોલર ઉષ્મા ............... $\mathrm{J\,mol}^{-1} \, \mathrm{K}^{-1}$View Solution
- 52અચળ તાપમાને કાર્બન ડાયોક્સાઈડ અને પાણી માં ઇથેનોલ માં દહન ઉષ્મા $-327\, kcal$ છે અચળ કદે અને $27^{\circ} C$ તાપમાને કેટલી ઉષ્મા મુક્ત થાય છે ?$\left( R =2\, cal\, mol ^{-1}\, K ^{-1}\right)$View Solution
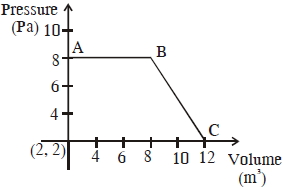
- 53એક આદર્શ વાયુ કે જે આકૃતિમાં દર્શાવેલા માર્ગ $ABC$ પર પ્રતિવર્તી વિસ્તરણ પામે છે તેના દ્વારા થતા કાર્યની માત્રા ............ થશે.View Solution
- 54જો $\mathrm{Br}_{2(l)}$ ની પરમાણ્વીયકરણ એન્થાલ્પી $\mathrm{x}\; \mathrm{kJ} / \mathrm{mol}$ અને $\mathrm{Br}_{2}$ માટે બંધ એન્થાલ્પી $y \;\mathrm{kJ} / \mathrm{mol}$ હોય તો તેઓ વચ્ચેનો સંબંધ જણાવો.View Solution
- 55જો ઇથેન, હાઇડ્રોજન અને ગ્રેફાઇટની દહન ઉષ્મા અનુક્રમે $-1560$, $-393.5$ અને $-286 \;\mathrm{kJ} / \mathrm{mol},$ હોય, તો ઇથેનની પ્રમાણિત સર્જન ઉષ્મા $\left(\Delta_{t} \mathrm{H}_{298}^{0}\right)$ .......... $kJ/mol$ જણાવો.View Solution
- 56$1$ બારના અચળ બાહ્ય દબાણ વિરુદ્ધ એક આદર્શ વાયુનુ $1\, L$ કદમાંથી $10\, L$ કદમાં વિસ્તરણ કરવામાં આવે છે. તો થયેલ કાર્ય $kJ$ માં ગણો.View Solution
- 57$4 \,Nm^{-2}$ ના અચળ બાહ્ય દબાણે, એક આદર્શ વાયુ $5\, m^3$ થી $1\, m^3$ સુધી સમતાપી સંકોચન પામે છે. આ પ્રક્રિયામાં ઉત્સર્જીત ઊષ્માનો ઊપયોગ $1$ મોલ $Al$ ને ગરમ કરવા માટે આવે છે. જો $Al$ ની મોલર ઊષ્મા ક્ષમતા $24\, J\, mol^{-1}K^{-1}$ હોય તો, $Al$ નું તાપમાન કેટલું વધશે?View Solution
- 58આપેલી રાસાયણિક પ્રક્રિયા $X\, \rightleftharpoons \,Y,$ માટે, પ્રમાણિત પ્રક્રિયા ગિબ્સ ઉર્જા તાપમાન $T $($K$ માં) પર નીચે મુજબ આધારિત છે.View Solution
${\Delta _r}{G^o}$ (in $kJ\,mol^{-1}$) $=120-\frac {3}{8}\,T$
તો $T$ તાપમાને પ્રક્રિયા મિશ્રણનો મુખ્ય ઘટક કયો?
- 59એક પ્રક્રિયામાં $\Delta H = 200\,J\,mo{l^{ - 1}}$ અને $\Delta S = 40\,J{K^{ - 1}}\,mo{l^{ - 1}}$ છે. નીચે આપેલી કિંમતો પૈકી કોઈ ઓછામાં ઓછું તાપમાન પસંદ કરો કે જેનાથી ઉપર પ્રક્રિયા......$K$ સ્વયંભૂ થશે?View Solution
- 60નિરપેક્ષ તાપમાન $T$ એ એક રાસાયણિક પ્રક્રિયા માટે પ્રમાણિત પ્રક્રિયા ગીબ્સ ઊર્જા નીચે મુજબ આપી શકાય,View Solution
${\Delta _r}{G^o} = A - BT$
જ્યાં $A$ અને $B$ શૂન્ય સિવાયના અચળાંકો છે. આ પ્રક્રિયા માટે નીચે આપેલા માંથી કયું સાચું છે?
- 61View Solutionનીચેના પૈકી ખોટી સરખામણી જણાવો.
- 62પ્રક્રિયા $2S{O_2}{\kern 1pt} (g)\, + \,{O_2}\,(g)\, \to \,2S{O_3}\,(g)$ માટેView Solution
${\Delta _H}\, = \, - 57.2\,kJ\,mo{l^{ - 1}}$ અને ${K_C} = 1.7\, \times \,{10^{16}}$ છે. નીચેના પૈકી ક્યુ વિધાન ખોટુ છે ?
- 63$100\, K$ પર રહેલા $5$ મોલ આદર્શ વાયુનું તાપમાન $200\, K$ થાય ત્યા સુધી તેનુ પ્રતિવર્તી સંકોચન કરવામાં આવે છે.View Solution
જો $C_v = 28 \, J\,K^{-1}\, mol^{-1}$ હોય તો $\Delta U$ અને $\Delta pV$ ગણો. $(R = 8.0\, J\, K^{-1}\, mol^{-1})$
- 64$200\,^oC$ તાપમાને આયોડિનની ઊર્ધ્વપાતન એન્થાલ્પી $24\, cal\, g^{-1}$ છે. જો $I_2(s)$ અને $I_2(vap)$ ની વિશિષ્ટ ઉષ્મા, અનુક્રમે $0.055$ અને $0.031\, cal\, g^{-1}K^{-1}$ હોય તો $250\,^oC$ તાપમાને આયોડિનની ઊર્ધ્વપાતન એન્થાલ્પી $cal\, g^{-1}$ માં ગણો.View Solution
- 65$273\, K$ એ $1\, kg$ બરફ ને $383\, K$ એ પાણીની વરાળ (બાષ્પ) માં રૂપાંતરિત કરવા માટે સંકળાયેલો એન્ટ્રોપી નો ફેરફાર કેટલો થાય? (પાણી (પ્રવાહી) અને પાણીની વરાળ (બાષ્પ) ની વિશિષ્ટ ઊષ્મા $4.2 \,kJ \,K^{-1}\,kg^{-1}$ અને $2.0\, kJ\,K^{-1}\,kg^{-1}$ પાણીની ગલન ઊષ્મા અને બાષ્પાયન ઊષ્મા અનુક્રમે $334 \,kJ\, kg^{-1}$ અને $2491\, kJ\, kg^{-1}$) ($log\, 273 = 2.436, log\, 373=2.572, log 383 = 2.583)$ .......$kJ\,K^{-1}\,kg^{-1}$View Solution
- 66$300\, K$ એ એક કોષનો પ્રમાણિત ઈલેક્ટ્રોડ પોટેન્શિયલ $E^-$ અને તેના તાપમાનનો સહ ગુણાંક $\left( {\frac{{d{E^ - }}}{{dT}}} \right)$ અનુક્રમે $2\,V$ અને $-5\times10^{-4}\, V\,K^{-1}$ છે. કોષ પ્રક્રિયાView Solution
$Zn\left( s \right) + C{u^{2 + }}\left( {aq} \right) \rightleftharpoons Z{n^{2 + }}\left( {aq} \right) + Cu\left( s \right)$
$300\,K$ એ પ્રમાણિત પ્રક્રિયા એન્થાલ્પી $\left( {{\Delta _r}{H^ - }} \right),\, kJ \,mol^{-1}$ માં કેટલા .............. $\mathrm{kJ}$ થશે?
$[R=8\,J\,K^{-1}\,mol^{-1}$ અને $F=96,000\,C\,mol^{-1}]$
- 67આપેલ ,View Solution
$(i)\,\,C\,({\rm{graphite}})\, + \,{O_2}{\kern 1pt} (g)\, \to \,C{O_2}\,(g);\,\Delta r{H^\circleddash} = x\,\,kJ\,mo{l^{ - 1}}$
$(ii)\,\,C\,({\rm{graphite}})\, + \,\frac{1}{2}{O_2}{\kern 1pt} (g)\, \to \,CO\,(g);\,\Delta r{H^\circleddash} = y\,\,kJ\,mo{l^{ - 1}}$
$(iii)\,\,CO\,(g)\, + \,\frac{1}{2}{O_2}{\kern 1pt} (g)\, \to \,C{O_2}\,(g);\,\Delta r{H^\circleddash} = z\,\,kJ\,mo{l^{ - 1}}$
ઉપરોક્ત, ઊષ્મારાસાયણિક સમીકરણો ના આધારે નીચેનામાંથી ક્યો બીજગણિતિક સંબંધ સાચો છે?
- 68View Solutionએક બંધ પ્રણાલીમાં દ્વિઆણ્વિય આદર્શ વાયુ માટે નીચે આપેલા આલેખો પૈકી કયો ઊષ્માગતિશાસ્ત્રના વિવિધ પરિમાણો વચ્ચેનો સાચો સંબંધ વર્ણવતો નથી?
- 69View Solutionજો….. હોય તો દરેક તાપમાને પ્રક્રિયા સ્વયંભૂ થશે ?
- 70જ્યારે એક મોલ હેપ્ટેન $(I)$ નું $T$ તાપમાને દહન કરવામાં આવે ત્યારે $\Delta H$ અને $\Delta U$ વચ્ચેનો તફાવત $(\Delta H - \Delta U),$ કોને સમાન થશે ?View Solution
- 71View Solutionનીચેના પૈકી ક્યુ સમીકરણ, આદર્શ વાયુને સમાવતા આપેલા પ્રક્રમ માટે ઉષ્માગતિશાસ્ત્રના પ્રથમ નિયમને રજૂ કરતું નથી ?
- 72નીચેના પૈકી માર્ગવિધેય (path function) રજૂ કરતો માપદંડોનો સેટ જણાવો.View Solution
$(a)\,\,q + w$ $ (b)\,\,q$
$(c)\,\,w$ $ (d)\,\,H -TS$
- 73View Solutionપ્રક્રમ જેમાં એન્ટ્રોપીમાં થતો ફેરફાર ઋણ છે.
- 74પ્રક્રિયા $MgO(s) + C(s) \to Mg(s) + CO(g)$ માટે $\Delta _r{H^o} = + 491.1\,kJ\,mo{l^{ - 1}}$ અને $\Delta _r{S^o} = 198.0\,Jk^{-1}\,mo{l^{ - 1}}$ જે $298\, K$ એ શક્ય નથી તો આ તાપમાનથી ઊપર .....$K$ તાપમાને પ્રક્રિયા શક્ય બનશે ?View Solution
- 75બે જુદા-જુદા તાપમાન $T_1$ અને $T_2$ એ એક બંધ પ્રણાલીમાં આદર્શ વાયુનું પ્રતિવર્તી સમતાપી વિસ્તરણ ધ્યાનમાં લો $(T_1 < T_2)$. અંતિમ કદ $(V)$ પર આધારિત થયેલા કાર્ય $(w)$ નું સચોટ આલેખીય વર્ણન નીચે પૈકી ક્યાં આલેખમાં છે?View Solution
- 76સરખી ધાતુના સરખા દળ ધરાવતા બે ટુકડાઓનું (બ્લોક) તાપમાન અનુક્રમે $T_1$ અને $T_2$ છે, તેમને એક બીજાના સંપર્કમાં લાવવામાં આવે છે અને અચળ દબાણ ઊષ્મીય સંતુલન પ્રાપ્ત કરવા દેવામાં આવે છે આ પ્રક્રિયા માટે એન્ટ્રોપી $\Delta S$ માં થતો ફેરફાર છે.View Solution
- 77સિલ્વર માટે ${C_P}\,\left( {J{K^{ - 1}}\,mo{l^{ - 1}}} \right) = 23 + 0.01\,T$ છે. જો $1\, atm$ દબાણે $3$ મોલ સિલ્વરનું તાપમાન $(T)$ એ $300\, K$ થી $1000\, K$ સુધી વધારવામાં આવે તો $\Delta H$ નું મૂલ્ય .....$kJ$ નજીક હશે ?View Solution
- 78સ્પ્રિંગના સંકોચન દરમિયાન $10\,kJ$ કાર્ય થાય છે અને $2\,kJ$ ઉષ્મા તરીકે પર્યાવરણમાં મુક્ત થાય છે. તો આંતરિક ઊર્જામાં થતો ફેરફાર $\Delta U$ ($kJ$ માં) જણાવો.View Solution
- 79$500\, K$ પર પદાર્થ $'S'$ માટે પ્રવાહી અવસ્થા અને વાયુઅવસ્થામાં ${\Delta _f}{G^o}$ અનુક્રમે $+100.7\, kcal\, mol^{-1}$ અને $+103\, kcal\, mol^{-1}$ છે. તો $500\, K$ પર પ્રવાહી $'S'$ નું બાષ્પદબાણ આશરે ..........$atm$ થશે. $(R\,= 2\,cal \,K^{-1}\,mol^{-1})$View Solution
- 80આપેલ:View Solution
$\left( i \right)\,2F{e_2}{O_3}\left( s \right) \to 4Fe\left( s \right) + 3{O_2}\left( g \right)$
${\Delta _r}{G^o} = + 1487.0\,kJ\,mo{l^{ - 1}}$
$\left( {ii} \right)\,2CO\left( g \right) + {O_2}(g) \to 2C{O_2}\left( g \right)$
${\Delta _r}{G^o} = - 514.4\,kJ\,mo{l^{ - 1}}$
તો નીચેની પ્રક્રિયા માટે મુક્ત ઊર્જા ફેરફાર $\Delta_rG^o$ .....$kJ\, mol^{-1}$
$\,2F{e_2}{O_3}\left( s \right) + 6CO\left( g \right) \to 4Fe\left( s \right) + 6C{O_2}\left( g \right)$
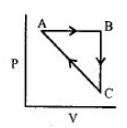
- 81એક આદર્શ વાયુ નીચે દર્શાવેલ આકૃતિ મુજબ ચક્રીય પ્રક્રમ અનુભવે છે.View Solution
$\Delta {U_{BC}} = - 5\,kJ\,mo{l^{ - 1}},{q_{AB}} = 2\,kJ\,mo{l^{ - 1}}$
$\Delta {W_{AB}} = - 5\,kJ\,mo{l^{ - 1}},{W_{CA}} = 3\,kJ\,mo{l^{ - 1}}$
$CA$ પ્રક્રમ દરમિયાન પ્રણાલી દ્વારા શોષાતી ઉષ્મા ......$kJ\,mo{l^{ - 1}}$
- 82નીચેના પૈકી કઈ પ્રક્રિયામાં માટે $\Delta H$ એ $\Delta U$ ને સમાન છે ?View Solution
- 83નીચેના પૈકી ક્યા પ્રક્રમ માટે$\Delta S$ ઋણ છે?View Solution
- 84$\Delta U$ નીચેના પૈકી કોને સમાન થશે ?View Solution
- 85$1\,$ મોલ પાણીનું $5\,^oC$ થી $-5\,^oC$ તાપમાને ઠારણ કરવાનો એન્થાલ્પી ફેરફાર.......$kJ\, mol^{-1}$View Solution
(Given ${\Delta _{fus}}H = 6\, kJ\, mol^{-1}$ at $0\,^oC$,
$C_p(H_2O, l) =75.3\, J\, mol^{-1} \, K^{-1}$ ,
$C_p(H_2O, s) = 36.8\, J\, mol^{-1} \, K^{ -1}$ )
- 86આપેલView Solution
$C_{(graphite)} +O_2(g) \rightarrow CO_2(g)\,;$ $\Delta _rH^o=-395.5 \, kJ\,mol^{-1}$
$H_2 (g) + \frac{1}{2} O_2 (g) \rightarrow H_2O(l)\,;$ $\Delta _rH^o =-285.8\, kJ\, mol^{-1}$
$CO_2(g) + 2H_2O(l) \rightarrow CH_4(g) + 2O_2(g)\,;$ $\Delta _rH^o = + 890.3\, kJ\, mol^{-1}$
ઉપર દર્શાવેલ થર્મોરાસાયણિક સમીકરણોને આધારે $298\, K$ તાપમાને પ્રક્રિયા $C_{(graphite)} + 2H_2(g) \rightarrow CH_4(g) $
માટે $\Delta_{r} H^{\circ}$ ની કિંમત ........... $kJ \,mol^{-1}$
- 87View Solutionએક આદર્શ વાયુ અચળ દબાણે સમતાપી વિસ્તરણ અનુભવે છે. આ પ્રક્રમ દરમિયાન ..
- 88એક વાયુ અવસ્થા $A$ માંથી અવસ્થા $B$ માં ફેરફાર અનુભવે છે. આ પ્રકમાં શોષાતી ઉષ્મા અને વાયુ દ્વારા થતુ કાર્ય અનુક્રમે $5\, J$ અને $8\, J$ છે. હવે વાયુને અન્ય પ્રક્રમ દ્વારા $A$માં લાવવામાં આવે છે, જે દરમિયાન $3\, J$ ઉષ્મા મુક્ત થાય છે.View Solution
આ $B$ થી $A$ ના પ્રતિગામી પ્રક્રમ માટે ...
- 89પ્રક્રિયા $A(g) \to A(l)$ માટે $\Delta H = - 3RT$ છે. તો પ્રક્રિયા માટે સાચો સંબંધ જણાવો.View Solution
- 90કાર્બન અને કાર્બન મોનોક્સાઇડની દહન ઉષ્માઓ અનુક્રમે $- 393.5$ અને $- 283.5\, kJ\, mol^{-1}$ છે. તો કાર્બન મોનોક્સાઇડની સર્જન ઉષ્મા (in $kJ$) શોધો.View Solution
- 91$1\,bar$ પર, એક પ્રક્રિયા નીચા તાપમાને બિનસ્વયંભૂ છે. પરંતુ ઊંચા તાપમાને રવયંભૂ બને છે. તો પ્રક્રિયા વિશે નીચેના પૈકી સાચુ વિધાન ઓળખો.View Solution
- 92જો $100\,$ મોલ $H_2O_2$ એ $1\, bar$ and $300\, K$ પર વિઘટન પામે તો $1$ મોલ $O_2(g)$ એ $1\, bar$ દબાણ વિરુદ્ધ પ્રસરણ પામેView Solution
ત્યારે થતુ કાર્ય ............$kJ$
$2{H_2}{O_2}(l) \rightleftharpoons {H_2}O(l) + {O_2}(g)$
$(R = 83\, JK^{-1}\, mol^{-1})$
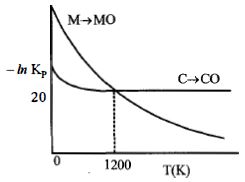
- 93નીચેનો આલેખ એ પ્રક્રિયાઓ $M(s) + \frac{1}{2}{O_2}(s)\, \to \,MO(s)\,$ અને $C(s) + \frac{1}{2}{O_2}(g)\, \to \,CO(s)\,$ માટે $- In\,K_p$ વિરુદ્ધ તાપમાનનો ફેરફાર દર્શાવે છે. તો સાયુ વિધાને ઓળખો.View Solution
- 94પ્રક્રિયા $A(g) + B(g) \to C(g) + D(g)$ માટે $298\,K$ પર $\Delta H^o$ and $\Delta S^o$ અનુક્રમે $-29.8\,\,kJ\, mol^{-1}$ અને $-0.100\,\,kJ\,K^{-1}$ $mol^{-1}$ છે $298\,K$ પર પ્રક્રિયાનો સંતુલન અચળાંક જણાવો.View Solution
- 95View Solutionનીચેના વિધાનો વાયુના ઘનની સપાટી પર અધિશોષણ સાથે સંકળાયેલા છે. તે પૈકી અસત્ય વિધાન ઓળખો.
- 96મિથેન અને ઇથેનની પરમાણ્વિયકરણ ઉષ્મા અનુક્રમે $360\,kJ/mol$ અને $620\,kJ/mol,$ છે. તો $C-C$ બંધ તોડવા જરૂરી સૌથી લાંબી તરંગલંબાઇ જણાવો. (એવોગેડ્રો આંક$ = 6.02 \times 10^{23},$ $h = 6.62 \times 10^{-34}\,Js$ )View Solution
- 97નીચે આપેલી પ્રક્રિયા $298 \,K$ તાપમાને કરવામાં આવી.View Solution
$2NO(g) + O_2(g) \rightleftharpoons 2NO_2(g)$
$298 \,K$ તાપમાને $NO(g)$ ની પ્રમાણિત સર્જન મુક્તઊર્જા $86.6\, kJ/mol$ છે. તો $298 \,K.$ તાપમાને $NO_2(g)$ ની પ્રમાણિત સર્જન મુક્તઊર્જા કેટલી થશે ? ($K_p = 1.6 \times 10^{12})$
- 98View Solutionબે ઘટકો A અને B ના આદર્શ દ્રાવણ માટે નીચેના પૈકી કયુ સાચુ છે?
- 99$1000\, K$ પર $CD_2O$ ની મોલર ઉષ્માક્ષમતા $(C_p)$ $10$ કેલરી છે. તો અચળ દબાણે $32\, g$ $CD_2O$ ને $1000\, K$ થી $100\, K$ તાપમાને ઠંડુ પાડવા સાથે સંકળાયેલ એન્ટ્રોપી ફેરફાર ....$cal\, deg^{-1}$. ($D\, =$ ડયુટેરિયમ, પરમાણ્વિય દળ $= 2\,u$ )View Solution
- 100$NH_3$ બનવાની પ્રમાણિત એન્થાલ્પી $-46.0\, kJ/mol$ છે.જો $H$ અણુથી $H_2$ સ્વરૂપ બનવાની એન્થાલ્પી એન્થાલ્પી $-436\, kJ/mol$ અને $N_2$ની $-712\, kJ/mol$ છે,$NH_3$માં $N - H$બંધ ની સરેરાશ બંધ એન્થાલ્પી......$kJ/mol$View Solution