$\mathrm{K}_{\mathrm{eq}}=\frac{\mathrm{k}_{\mathrm{f}}}{\mathrm{k}_{\mathrm{b}}}=\frac{\left[\mathrm{N}_{2}\right]\left[\mathrm{H}_{2} \mathrm{O}\right]^{2}}{\left[\mathrm{H}_{2}\right]^{2}[\mathrm{NO}]^{2}}$
At equilibrium $\mathrm{r}_{\mathrm{f}}=\mathrm{r}_{\mathrm{b}}$
$\mathrm{k}_{\mathrm{f}}\left[\mathrm{H}_{2}\right][\mathrm{NO}]^{2}=\mathrm{k}_{\mathrm{b}} \frac{\left[\mathrm{N}_{2}\right]\left[\mathrm{H}_{2} \mathrm{O}\right]^{2}}{\left[\mathrm{H}_{2}\right]}$
Hence, rate expression for reverse reaction.
$=\mathrm{k}_{\mathrm{b}} \frac{\left[\mathrm{N}_{2}\right]\left[\mathrm{H}_{2} \mathrm{O}\right]^{2}}{\left[\mathrm{H}_{2}\right]}$
Download our appand get started for free
Similar Questions
- 1$H_2 + I_2 $ $\rightleftharpoons$$H_I$ પ્રક્રિયા માટે સાચો સંબંધ લખો.View Solution
- 2$2N_2O_5 \rightarrow 4NO_2 + O_2$ પ્રક્રિયા માટે જો $NO_2$ ની સાંદ્રતા $1.6 × 10^{-2}$ સેકન્ડમાં વધે છે તો $ NO_2$ નો નિર્માણ દર.....View Solution
- 3જો $87.5\% $ નો કોઈપણ આપેલ પદાર્થનું $40$ મિનિટમાં વિભંજન થાય તો રેડીયો એક્ટિવ પદાર્થની અદ્ય આયુ કેટલી થાય છે?View Solution
- 4View Solutionનીચેના ગ્રાફ માટે,
નીચે આપેલા વિકલ્પોમાંથી પસંદ કરો, પ્રક્રિયાના ક્રમમાં કયો સંબંધિત સાચો છે:
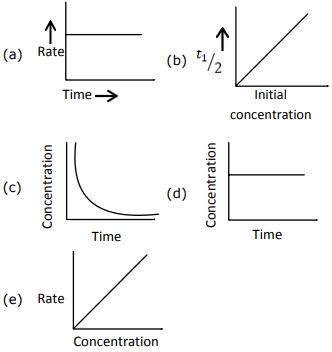
- 5$A$ તથા $B$ વચ્ચેની પ્રક્રિયામાં $A$ ના સંદર્ભમાં પ્રક્રિયાક્રમ $2$ છે. તથા $B$ ના સંદર્ભમાં પ્રક્રિયાક્રમ $3$ છે. જો $A$ તથા $B$ બંનેની સાંદ્રતા બમણી કરવામાં આવે તો પ્રક્રિયાક્રમ .............. ના ગુણકથી વધશે.View Solution
- 6નીચે આપેલામાંથી ખોટા વિધાન/નો ની સંખ્યા $........$ છે.View Solution
$A$. શૂન્ય ક્રમની પ્રક્રિયાઆના અનુગામી અર્ધ આયુષ્ય સમય સાથે ધટે છે.
$B$. રાસાયણિક સમીકરણ પ્રક્રિયક તરીકે દેખાતો પદાર્થ પ્રક્રિયાના (પ્રક્રિયાવેગને)દરને અસર કરી શકે નહી.
$C$. એક રાસાયણિક પ્રક્રિયાની આણિવક્તા અને ક્રમ અપૂર્ણાક સંખ્યા હોઈ શકે છે.
$D$. શૂન્ય અને દ્વિતિય ક્રમ પ્રક્રિયાનો વેગ અચળાંક અનુક્રમે $mol\,L ^{-1}\,s ^{-1}$ અને $mol ^{-1}\,L$ $s^{-1}$ છે.
- 7આર્હેંનિયસ સમીકરણ મુજબ, તેની રાસાયણિક પ્રક્રિયા $(\log \,k) $ નો દર અચળાંકનો લોગેરીયમ આલેખ દ્વારા સીધી રેખા દર્શાવવામાં આવી છે. તેને કઈ રીતે દર્શાવાય.View Solution
- 8$3/4$ જેટલી પુરી થવા માટે પ્રથમ ક્રમની પ્રક્રિયાને કેટલો સમય લાગે ?View Solution
- 9ઓઝોનને ગરમ કરવાથી તેનુ ઓક્સિજનમાં નીચે મુજબ વિધટન થાય છે.View Solution
${O_3} \rightleftharpoons {O_2} + \left[ O \right]$
${O_3} + \left[ O \right] \to 2{O_2}$ (slow)
તો $2{O_3} \to 3{O_2}$ પ્રક્રિયાનો કમ જણાવો.
- 10આપેલ પ્રક્રિયા $2NO + {O_2} \to 2N{O_2}$ કઈ પ્રક્રિયાનું ઉદાહરણ છે?View Solution
